时间:2021-02-18 04:54:18
1、选择题 配制一定物质的量浓度的某溶液,下列情况会使配制溶液浓度偏高的是( )
A.转移时有少量溶液洒到外面
B.容量瓶中原来含有少量蒸馏水
C.未洗涤烧杯和玻璃棒
D.定容时俯视刻度线观察液面
2、选择题 VmlAl2(SO4)3溶液中含Al3+ag,取V/4ml溶液稀释到4Vml,则稀释后溶液中SO的物质的量浓度是 ( )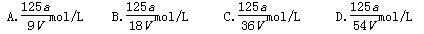
3、选择题 下列各组物质中,所含分子数相同的是
[? ]
4、选择题 设NA为阿伏加德罗常数的值。下列说法正确的是(?)
A.常温常压下,17g甲基(―14CH3)所含的中子数为9NA
B.标准状况下,将2.24L Cl2溶于水,可得到HClO分子的数目是0.1NA
C.42.0 g乙烯和丙烯的混合气体中含有的碳原子数为3NA
D.5.6g铁与0.1mol氯气在点燃条件下充分反应,转移的电子数为0.3NA
5、选择题 常温下c(H+)最小的是( )
A.pH=0的溶液.
B.0.04?mol?L-1?的H2SO4.
C.0.5?mol?L-1?的HCl.
D.0.05?mol?L-1的HNO3