ʱ��:2021-02-18 04:41:29
1������� A��B��C��D��E��F ���ֶ���������Ԫ�ص�ԭ����������������֪��
��A��B���γɶ�����̬�����B��D���γ����ֳ�����̬�����D��E���γ��������ӻ����
��B��C��D��ͬһ�������ڵ�����Ԫ�أ�����C��E��ԭ������֮�͵���A��F��ԭ������֮�ͣ�
��EԪ�ص�ԭ�Ӱ뾶����FԪ�ص�ԭ�Ӱ뾶��
��ش�
��1��EԪ����Ԫ�����ڱ���λ����______��E��D��ԭ�Ӹ���Ϊ1��1�γɵĻ�����ĵ���ʽ��______�������Ļ�ѧ����______��
��2��B��D�γɵ�������̬�������к�������ԭ�ӵĻ�����Ľṹʽ��______������ͨ������NaAlO2��Һ��������______�����ӷ���ʽΪ______��
��3����A��C��F����Ԫ�������һ�����ӻ���������������ӵķ����ǣ������ӷ���ʽ��ʾ��______��
��4��������ͬ��ԭ��������ͬ�ĵ������IJ�ͬ���ӳ�Ϊ�ȵ����壮д������������Ԫ���γɵ���������CԪ�صĵ��ʻ�Ϊ�ȵ������һ�����ӵĻ�ѧʽ��______��
�ο��𰸣�A��B��C��D��E��F���ֶ���������Ԫ�ص�ԭ��������������A��B���γɶ�����̬�������AΪH��BΪC��B��D���γ����ֳ�����̬�������DΪO��D��E���γ��������ӻ��������EΪNa��B��C��D��ͬһ�������ڵ�����Ԫ�أ���CΪN��C��E��ԭ������֮�͵���A��F��ԭ������֮�ͣ�����F��ԭ������Ϊ7+11-1=17������FΪCl��
��1��Naλ��Ԫ�����ڱ��е������ڵڢ�A�壬��O��ԭ�Ӹ���Ϊ1��1�γɵĻ�����ΪNa2O2�������ʽΪ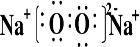
���������Ӽ����ۼ���
�ʴ�Ϊ���������ڵڢ�A�壻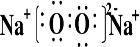
�����Ӽ����ۼ���
��2��B��D�γɵ�������̬�������к�������ԭ�ӵĻ�����ΪCO2����ṹʽΪO=C=O������ͨ������NaAlO2��Һ��Ӧ��������������������۲쵽��ɫ���������ӷ�Ӧ����ʽΪ
CO2+2AlO2-+3H2O�T2Al��OH��3��+CO32-���ʴ�Ϊ��O=C=O����ɫ�������ɣ�CO2+2AlO2-+3H2O�T2Al��OH��3��+CO32-��
��3��A��C��F����Ԫ�������һ�����ӻ�����ΪNH4F��һ��������Ӧ���ɰ��������飬���ӷ�ӦΪNH4++OH-?��?.?NH3��+H2O��
�ʴ�Ϊ��NH4++OH-?��?.?NH3��+H2O��
��2��������ͬ��ԭ��������ͬ�ĵ������IJ�ͬ���ӳ�Ϊ�ȵ����壬N2��ԭ����Ϊ2��������Ϊ7��2=14����CO��ԭ����Ϊ2��������Ϊ6+8=14������Ϊ�ȵ����壬�ʴ�Ϊ��CO��
���������
�����Ѷȣ�һ��
2������� ��A��B��C��D����Ԫ�أ�AԪ���ǵؿ��к������Ľ���Ԫ�أ�BԪ�ص�ԭ����M���������L����1�����ӣ�CԪ�ص�ԭ�ӵõ�2�����ӣ�DԪ�ص�ԭ��ʧȥ1�����ӣ����õ���������������ԭ����ͬ�ĵ��Ӳ�ṹ���ش��������⣺
��1����������Ԫ�ص����Ʒֱ���A______B______C______D______��
��2������A���ӡ�Cԭ�ӵĽṹʾ��ͼ______��______��
�ο��𰸣�A��B��C��D����Ԫ�أ�AԪ���ǵؿ��к������Ľ���Ԫ�أ���AΪAlԪ�أ�BԪ�ص�ԭ����M���������L����1�����ӣ���M�������Ϊ8-1=7����BΪClԪ�أ�CԪ�ص�ԭ�ӵõ�2�����ӣ�DԪ�ص�ԭ��ʧȥ1�����ӣ����õ���������������ԭ����ͬ�ĵ��Ӳ�ṹ����Cԭ�Ӻ��������Ϊ10-2=8��ΪOԪ�أ�DԪ��ԭ�Ӻ��������Ϊ10+1=11����DΪNaԪ�أ�
��1��������������֪��AΪ����BΪ�ȣ�CΪ����DΪ�ƣ��ʴ�Ϊ�������ȣ������ƣ�
��2��A����ΪAl3+�����������Ϊ10����2�����Ӳ㣬����������Ϊ8�����ӽṹʾ��ͼΪ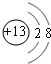
��
CΪ��Ԫ�أ�ԭ�Ӻ��������Ϊ8��ԭ�ӽṹʾ��ͼΪ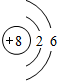
��
�ʴ�Ϊ��
��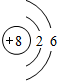
��
���������
�����Ѷȣ���
3������� ��������Ԫ�ػ�̬ԭ�ӵĵ����Ų������ж�Ԫ�أ����ش����⡣
A��ԭ����ֻ��һ���ܲ���ֻ��1 �����ӣ�B��ԭ��3p����ϵõ�1�����Ӻ����������������ӣ�C��ԭ�ӵ�2p�������1�����ӵ������������������ӵ����������෴��D��ԭ�ӵ����ܲ�����8�����ӣ������ܲ���ֻ��1�����ӣ�Eԭ�ӵ���Χ�����Ų�Ϊ3s23p6��
��1��д����A��B��C��D�е�����Ԫ����ɵĻ�����Ļ�ѧʽ������д��2������______________��
��2��д��������Ԫ����ɵ������Ƶ�A�ĵ��ʵĻ�ѧ����ʽ������д��1������___________________��
��3������ij��Һ���Ƿ���D+�����ӣ���ͨ��______________��Ӧ��ʵ�֣�����ij��Һ���Ƿ���B-�����ӣ�ͨ�����õ�����_________��_______��
��4��д��E��Ԫ�ط���___________��Ҫ֤��̫�����Ƿ���EԪ�أ��ɲ��õķ�����______________________��
�ο��𰸣����ԡ�
���������
�����Ѷȣ�һ��
4��ѡ���� X��Y��Z��WΪ���ڱ���ǰ20��Ԫ���е����֣�ԭ��������������W��YΪ����Ԫ�أ�Xԭ�ӵ������������Ǵ�����������3����Y��Zλ��ͬ���ڣ�Z������һ�����õİ뵼�壮W������ˮ���ҷ�Ӧ��Y��Zԭ�ӵ�����������֮����X��Wԭ�ӵ�����������֮����ȣ�����˵����ȷ���ǣ�������
A��ԭ�Ӱ뾶��W��Y��Z��X
B����̬�⻯����ȶ��ԣ�X��Z
C������������Ӧˮ����ļ��ԣ�Y��W
D��Y��Z�������ﶼ�����Ժͼ���
�ο��𰸣�X��Y��Z��WΪ���ڱ���ǰ20��Ԫ���е����֣�ԭ��������������Xԭ�ӵ������������Ǵ�����������3������X��3�����Ӳ㣬����������Ϊ6����XΪ��Ԫ�أ�Z������һ�����õİ뵼�壬ZΪ��Ԫ�أ�W��YΪ����Ԫ�أ�Y��Zλ��ͬ���ڣ�Y��Zԭ�ӵ�����������֮����X��Wԭ�ӵ�����������֮����ȣ���Y������������Ϊ3��W������������Ϊ1����YΪ��Ԫ�أ�ԭ������W���ڹ�Ԫ�أ���WΪ��Ԫ�أ���������ˮ���ҷ�Ӧ����XΪ��Ԫ�أ�YΪ��Ԫ�أ�ZΪ��Ԫ�أ�WΪ��Ԫ�أ�
A��ͬ������ԭ����������ԭ�Ӱ뾶��С������ԭ�Ӱ뾶Na��Al��Si��C��O��ͬ�������϶��£�ԭ�Ӱ뾶��������ԭ�Ӱ뾶K��Na��Si��C������ԭ�Ӱ뾶K��Al��Si��O����W��Y��Z��X����A��ȷ��
B��XΪ��Ԫ�أ�ZΪ��Ԫ�أ�ͬ�������϶��·ǽ����Լ��������Էǽ�����O��Si���ǽ�����Խǿ���⻯��Խ�ȶ���������̬�⻯���ȶ���X��Y����B����
C��YΪ��Ԫ�أ�WΪ��Ԫ�أ�ͬ�������϶��½�������ǿ�����Խ�����K��Na��ͬ����������ҽ����Լ��������Խ�����Na��Al��������K��Al��������Խǿ������������Ӧˮ����ļ���Խǿ�����Լ���Y��W����C����
D��YΪ��Ԫ�أ�ZΪ��Ԫ�أ���������������������������������������D����
��ѡA��
���������
�����Ѷȣ�һ��
5��ѡ���� X��Y��ZΪ���ֵ��ʣ���֪��Y�ܽ�Z���仯�����ˮ��Һ���û���������Z���ܽ�X���仯�����ˮ��Һ���û��������ɴ˿����ƶ�����˵���п�����ȷ���ǣ�������
�ٵ��ʵ������ԣ�Y��Z��X��?�ڵ��ʵĻ�ԭ�ԣ�Y��Z��X��
�۶�Ӧ���ӵ������ԣ�X��Z��Y��?�ܶ�Ӧ���ӵĻ�ԭ�ԣ�X��Z��Y��
A��ֻ�Т�
B��ֻ�Тڢ�
C��ֻ�Т٢�
D���٢ڢۢ�
�ο��𰸣�������Ϊ�ǽ�����Y�ܽ�Z���仯�����ˮ��Һ���û���������Z���ܽ�X���仯�����ˮ��Һ���û�����������������������ǿ���������������ԣ����ʵ������ԣ�Y��Z��X���ʢ���ȷ��
������Ϊ������Y�ܽ�Z���仯�����ˮ��Һ���û���������Z���ܽ�X���仯�����ˮ��Һ���û����������û�ԭ����ԭ��ǿ�ڻ�ԭ����Ļ�ԭ�ԣ����ʵĻ�ԭ�ԣ�Y��Z��X���ʢ���ȷ��
������Ϊ���������ʵĻ�ԭ�ԣ�Y��Z��X����ԭ��Խǿ������������Խ�������Ӧ���ӵ������ԣ�X��Z��Y���ʢ���ȷ��
������Ϊ�ǽ��������ʵ������ԣ�Y��Z��X��������Խǿ��Ӧ�����ӵĻ�ԭ��Խ������Ӧ���ӵĻ�ԭ�ԣ�X��Z��Y���ʢ���ȷ��
��ѡD��
���������
�����Ѷȣ���