时间:2021-02-18 04:31:25
1、选择题 下列各组物质能用分液漏斗进行分离的是
A.汽油和四氯化碳
B.碘与四氯化碳
C.酒精与汽油
D.水与苯
参考答案:D
本题解析:分液要两种溶剂互不相容,汽油和四氯化碳、碘与四氯化碳、酒精与汽油?都是互溶的,不可以分液。
本题难度:一般
2、填空题 苯甲酸广泛应用于制药和化工行业,某同学尝试用甲苯的氧化反应制备苯甲酸,反应原
理:
实验方法:一定量的甲苯和适量的KMnO4溶液在100℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯。
已知:苯甲酸相对分子质量122 ,熔点122.4℃,在25℃和95℃时溶解度分别为0.3 g和6.9 g;纯净固体有机物一般都有固定熔点。
(1)操作Ⅰ为 ?,需要用到的主要玻璃仪器为 ??;操作Ⅱ为 ?。
(2)无色液体A是?,定性检验A的试剂是 ?,现象是?。
(3)测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确.请在答题卡上完成表中内容。
| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 将白色固体B加入水中, 加热溶解,?? | 得到白色晶体和无色溶液 | ? |
| ② | 取少量滤液于试管中, ? | 生成白色沉淀 | 滤液含Cl- |
| ③ | 干燥白色晶体,? | ?? | 白色晶体是苯甲酸 |
参考答案:(1)分液(1分),分液漏斗、烧杯等(1分);蒸馏(1分)
(2)甲苯(1分);酸性KMnO4溶液(1分),溶液褪色(1分)(3)
序号
实验方案
实验现象
结论
①
将白色固体B加入水中加热,溶解,冷却结晶、过滤 (2分)
得到白色晶体和无色溶液
?
②
取少量滤液于试管中,滴入2-3滴硝酸酸化的AgNO3溶液(2分)
生成白色沉淀
滤液含有Cl-
③
干燥白色晶体,加热使其融化,测其熔点(2分)
熔点为122.4℃(2分)
白色晶体是苯甲酸
?
(4)(2.40×10-3×122×4)/1.22(2分);96%(2分)
本题解析:(1)一定量的甲苯和KMnO4溶液在100℃反应一段时间后停止反应,按流程分离出苯甲酸和回收未反应的甲苯;所以操作Ⅰ是分离出有机相甲苯,用分液方法得到,分液操作的主要玻璃仪器是分液漏斗、烧杯等;操作Ⅱ是蒸馏的方法控制甲苯沸点得到纯净的甲苯液体;
(2)依据流程和推断可知,无色液体A为甲苯,检验试剂可以用酸性高锰酸钾溶液,甲苯被氧化为苯甲酸,高锰酸钾溶液紫色褪去;
(3)通过测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,推测白色固体B是苯甲酸与KCl的混合物,氯化钾可以用硝酸酸化的硝酸银溶液检验氯离子的存在;利用苯甲酸的溶解度特征在25℃和95℃时溶解度分别为0.3g和6.9g;利用不同温度下的溶解度,分离混合物,得到晶体后通过测定熔点判断是否为苯甲酸;
(4)称取1.220g产品,配成100ml甲醇溶液,移取25.00ml溶液,滴定,消耗KOH的物质的量为2.40×10-3mol,苯甲酸是一元弱酸和氢氧化钾1:1反应,所以物质的量相同,则样品中苯甲酸质量分数=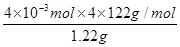 ×100%=96%。
×100%=96%。
本题难度:一般
3、选择题 下列除杂方案错误的是
| 选项 | 被提纯的物质 | 杂质 | 除杂试剂 | 除杂方法 |
| A. | CO(g) | CO2(g) | NaOH 溶液、浓H2SO4 | 洗气 |
| B. | NH4Cl(aq) | Fe3+(aq) | NaOH溶液 | 过滤 |
| C. | Cl2(g) | HCl(g) | 饱和食盐水、浓H2SO4 | 洗气 |
| D. | Na2CO3(s) | NaHCO3(s) | ― | 灼烧 参考答案:B 本题解析:A项依次通过NaOH 溶液、浓 H2SO4,分别除去CO2,水蒸气,正确;B项NaOH溶液与NH4Cl也反应,错误;C项依次通过饱和食盐水、浓H2SO4,分别除去HCl,水蒸气,正确;D项通过灼烧能使NaHCO3固体分解生成Na2CO3,正确。 本题难度:一般 4、选择题 下列有机物检验方法正确的是 参考答案:C 本题解析:A错,取少量卤代烃加入NaOH水溶液共热,冷却,加入稀硝酸酸化,再加入AgNO3溶液检验卤代烃中卤原子的存在;B错,乙醇与乙烯均能使酸性高锰酸钾溶液褪色;C正确;D错,用 本题难度:一般 5、选择题 下列各组物质能用过滤的方法分离的是( ) 参考答案:B 本题解析:过滤的方法分离的是固体和液体的混合物,只有B合适 本题难度:一般 |