时间:2021-02-18 04:29:57
1、选择题 1966年美国福特汽车公司首次发表了Na-S电池的有关报导。其结构如图所示,电池反应为2Na+ S8
S8 Na2Sn。下列说法不正确的是
Na2Sn。下列说法不正确的是
A.熔钠电极作电池的正极
B.放电时Na+向正极移动
C.充电时熔钠电极与电源的负极相连
D.充电时阳极反应式为8Sn2-―16e-=nS8
参考答案:A
本题解析:A、钠失去电子,为负极,错误;B、原电池中正电荷向正极移动,正确;C、可逆电池中放电时的负极,充电时为阴极,形成物质可逆,正确;D、根据总反应方程式判断,正确。
本题难度:一般
2、选择题 下列叙述正确的是
①原电池是将化学能转化为电能的一种装置?
②原电池的正极发生氧化反应,负极发生还原反应?
③不能自发进行的氧化还原反应,通过原电池装置可以实现?
④碳棒不能用来作原电池的正极?
⑤反应Cu+2Ag+?= Cu2++2Ag?能以原电池的形式实现
A.②⑤
B.①④⑤
C.②③④
D.①⑤
参考答案:D
本题解析:原电池的正极发生还原反应,负极发生氧化反应,②不正确。只有自发进行的氧化还原反应,才能通过原电池装置实现,③不正确。④不正确,碳棒可以导电,可用作电极,所以正确的答案是①⑤,答案选D。
本题难度:简单
3、选择题 镉镍可充电电池在现代生活中有广泛应用,它的充、放电反应按下式进行:Cd+2NiOOH+2H2O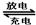 Cd(OH)2+2Ni(OH)2 ,由此判断错误的是:( ?)
Cd(OH)2+2Ni(OH)2 ,由此判断错误的是:( ?)
A.放电时,Cd作负极
B.放电时,NiO(OH)作负极
C.电解质溶液为碱性溶液
D.放电时,负极反应为Cd+2OH--2e-=Cd(OH)2
参考答案:B
本题解析:A.由方程式Cd+2NiOOH+2H2O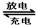 Cd(OH)2+2Ni(OH)2可知,放电时,Cd元素化合价升高,被氧化,在原电池负极上发生氧化反应,则Cd为原电池的负极,错误;B.由A可知正确;C.依据电池反应分析判断,电池是碱性电池,错误;D.放电时负极上发生的电极反应式为:Cd-2e-+2OH-=Cd(OH)2,错误。
Cd(OH)2+2Ni(OH)2可知,放电时,Cd元素化合价升高,被氧化,在原电池负极上发生氧化反应,则Cd为原电池的负极,错误;B.由A可知正确;C.依据电池反应分析判断,电池是碱性电池,错误;D.放电时负极上发生的电极反应式为:Cd-2e-+2OH-=Cd(OH)2,错误。
本题难度:简单
4、选择题 下图所示装置能够组成原电池,并且能产生明显电流的是的是( )
A.
稀硫酸
B.
稀硫酸
C.
硫酸铜
D.
乙醇
参考答案:A.两电极相同,不能形成原电池,故A错误;
B.没有形成闭合回路,不能形成原电池,故B错误;
C.锌为负极,铜为正极,可形成原电池反应,故C正确;
D.乙醇为非电解质,不导电,不能形成原电池,故D错误.
故选C.
本题解析:
本题难度:简单
5、选择题 为探究原电池的形成条件和反应原理,某同学设计了如下实验并记录了现象:①向一定浓度的稀硫酸中插入锌片,看到有气泡生成;②向上述稀硫酸中插入铜片,没有看到有气泡生成;③将锌片与铜片上端接触并捏住,一起插入稀硫酸中,看到铜片上有气泡生成,且生成气泡的速率比实验①中快;④在锌片和铜片中间接上电流计,再将锌片和铜片插入稀硫酸中,发现电流计指针偏转.下列关于以上实验设计及现象的分析,不正确的是( )
A.实验①、②说明锌能与稀硫酸反应而铜不能
B.实验③说明发生原电池反应时会加快化学反应速率
C.实验③说明在该条件下铜可以与稀硫酸反应生成氢气
D.实验④说明该原电池中铜为正极、锌为负极
参考答案:①锌为活泼金属,能与硫酸发生置换反应生成氢气;
②铜为金属活动性顺序表中H以后的金属,不与稀硫酸反应;
③当锌和铜连接插入稀硫酸中,能形成原电池,锌较活泼,作原电池的负极,负极材料不断消耗,铜较不活泼,作原电池的正极,电极上有气泡产生,且原电池反应较一般的化学反应速率较大,反应的实质是氢离子在铜极上得电子被还原产生氢气;
④活泼性不同的锌、铜以及电解质溶液形成闭合回路时,形成原电池,将化学能转变为电能,电流计指针偏转.
不正确的只有③,
故选C.
本题解析:
本题难度:简单