时间:2020-08-23 08:26:47
1、选择题 2011年3月11日,日本大地震引起全世界关注,中国核事故应急协调委员会4月1曰发布,内地除西藏外都检测到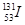 ,还检测到了极微量的人工放射性核素
,还检测到了极微量的人工放射性核素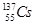 、
、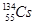 。已知铯(Cs)是钠的同族元素,据此,下列关说法正确的是(?)
。已知铯(Cs)是钠的同族元素,据此,下列关说法正确的是(?)
A.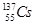 、
、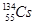 互为同位素
互为同位素
B.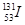 放出射线是一个自发的化学变化过程,射线对人危害很大
放出射线是一个自发的化学变化过程,射线对人危害很大
C.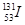 与
与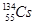 的中子数相同
的中子数相同
D.单质铯的金属性比单质钠弱
参考答案:A
本题解析: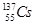 、
、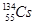 质子数相同,中子数不同,互为同位素,A选项正确;
质子数相同,中子数不同,互为同位素,A选项正确;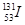 放出射线是一个物理变化,B选项不正确;
放出射线是一个物理变化,B选项不正确;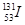 的中子数为131-53=78,
的中子数为131-53=78,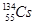 的中子数为134-55=79,C选项不正确;铯原子半径大,对电子作用力小,易失去,单质铯的还原性比单质钠强D选项不正确。
的中子数为134-55=79,C选项不正确;铯原子半径大,对电子作用力小,易失去,单质铯的还原性比单质钠强D选项不正确。
本题难度:一般
2、选择题 贴有下列危险品标志的药品起火时,不能用水灭火的是
A.剧毒品
B.遇湿易燃物品
C.腐蚀品
D.有害品(远离食品)
参考答案:B
本题解析:分析:药品起火时,以下四种物质的火灾不能用水扑救:
(1)比水轻的易燃液体火灾,如汽油,煤油等火灾,不能用水扑灭.因为水比油的比重大,油浮于水面之上仍能继续燃烧.
(2)容易被损坏的物质,如图书,档案和精密仪器等不能用水扑救.
(3)对于高压电器火灾是不能用直流水扑救的,因为水具有一定的导电性.
(4)与水起化学反应,分解出可燃气体或产生大量热能的物质,如钾,钠,钙,镁等轻金属和电石等物质的火灾,禁止使用水扑救.
结合各标志的含义进行分析判断.
解答:A.图中所示标志是有毒气体标志,有毒气体起火时能用水来灭火,故A错误;
B.图中所示标志是遇湿易燃物品标志,起火时不能用水灭火,故B正确;
C.图中所示标志是腐蚀品标志,腐蚀品起火时能用水来灭火,故C错误;
D.图中所示标志是有害品(远离食品)标志,有害品(远离食品)起火时能用水来灭火,故D错误.
故选B.
点评:本题考查危险品标志,难度不大,了解起火时,不能用水灭火的物质的性质、各个标签所代表的含义是解答本题的关键.
本题难度:一般
3、选择题 砷为第四周期第ⅤA族元素,则砷不可能具有的性质:?
A.砷通常情况下是固体
B.砷可以有-3、+3、+5等多种化合价
C.As2O5对应水化物酸性比H3PO4弱
D.砷的非金属性比磷强
参考答案:D
本题解析:略
本题难度:简单
4、选择题 已知E与G反应生成L和M,且组成E、G、L、M分子的元素原子序数均小于10,用它们的结构式表示反应如下图所示。则下列判断错误的是( )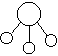 ?+
?+ 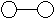 ?
?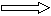 ?
?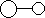 ?+
?+ 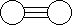
E? G? L? M
A.G是最活泼的非金属单质
B.L分子中有共价键
C.E能使紫色石蕊试液变蓝色
D.M化学性质很活泼
参考答案:D
本题解析:根据题意可以推断出E为氨气,G为氟气,L为氟化氢,M为氮气,所以G是最活泼的非金属单质,故A正确;L分子中有共价键,故B正确;E能使紫色石蕊试液变蓝色,故C正确;M化学性质不活泼,故D错误,为本题的正确答案。
点评:本题考查了非金属及其化合物,该考点是高考考查的重点和难点,本题采用的形式比较新颖,该题难度适中。
本题难度:简单
5、选择题 X元素的简单阳离子和Y元素的简单阴离子具有与氩原子相同的电子层结构。下列叙述正确的是(? )
A.X的原子序数比Y的小
B.X原子的电子层数比Y的少
C.X的原子半径比Y的小
D.X元素的最高正价比Y的小
参考答案:D
本题解析:X元素的简单阳离子和Y元素的简单阴离子具有与氩原子相同的电子层结构,说明Y元素在X元素的上一周期,X的原子序数比Y的大。
本题难度:简单