ʱ��:2020-08-23 08:20:08
1��ѡ���� ��֪�ڳ����²��Ũ�Ⱦ�Ϊ0.1 mol��L-1������������Һ��pH��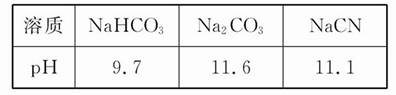
����˵������ȷ����(? )
A�������ӵ����ʵ���Ũ��֮�ͣ�Na2CO3��NaCN��NaHCO3
B����ͬ�����µ����ԣ�H2CO3<HCN
C��������Һ�о����ڵ���ƽ���ˮ��ƽ��
D������Na2CO3��Һ���¶ȣ� ��С
��С
�ο��𰸣�C
��������������Ӿ�ΪNa+��H+��Na2CO3��Һ��Na+Ũ��������������Һ��������������Ũ�����NaCN��Һ��NaHCO3��Һ��Na+Ũ����ȣ�NaCN��Һ��H+Ũ��С��NaHCO3��Һ����������Ũ�ȴ�С˳��ΪNa2CO3��NaHCO3��NaCN��A�����HCO3-��ˮ������С��CN-�������ԣ�H2CO3��HCN��B���������Na2CO3��Һ���¶ȣ��ٽ���ˮ�⣬ ����D�����
����D�����
�����Ѷȣ�һ��
2��ѡ���� �������ӷ���ʽ��ȷ���ǣ�?��
A������ˮ�� S2-+2H2O H2S+2OH-
H2S+2OH-
B�����⻯�Ƶ�ˮ�� HS-+H2O H3O++S2-
H3O++S2-
C�����ϼ�������Ȼ�����Һ Fe3++3H2O Fe(OH)3+3H+
Fe(OH)3+3H+
D����������Һ��NaHCO3��Һ��Ӧ Al3++3HCO3-=Al(OH)3��+3CO2��
�ο��𰸣�D
���������A����Ԫ��������ӷֲ�ˮ�⣬����ˮ��? S2-+H2O HS�D +OH-,?A����B�����⻯�Ƶ�ˮ��ӦΪ��HS-+H2O
HS�D +OH-,?A����B�����⻯�Ƶ�ˮ��ӦΪ��HS-+H2O H2S��OH�D�� HS-+H2O
H2S��OH�D�� HS-+H2O H3O++S2-�ǵ��뷽��ʽ��B����C�����ϼ�������Ȼ�����Һ��Fe3�� ��ˮ����ȫ�����ɳ�����Fe3++3H2O
H3O++S2-�ǵ��뷽��ʽ��B����C�����ϼ�������Ȼ�����Һ��Fe3�� ��ˮ����ȫ�����ɳ�����Fe3++3H2O Fe(OH)3��+3H+��C����D����������Һ��NaHCO3��Һ��Ӧ? Al3++3HCO3-=Al(OH)3��+3CO2����˫ˮ�⣬D��ȷ��
Fe(OH)3��+3H+��C����D����������Һ��NaHCO3��Һ��Ӧ? Al3++3HCO3-=Al(OH)3��+3CO2����˫ˮ�⣬D��ȷ��
ѡD��
�����Ѷȣ�һ��
3��ѡ���� ������0��1mol/L CH3COONa��Һ�зֱ��������NH4NO3��Na2SO3��FeCl3���壨������Һ����仯������CH3COO-Ũ�ȵı仯����Ϊ
[? ]
A����С������С
B������С����С
C��������������
D������������
�ο��𰸣�A
���������
�����Ѷȣ�һ��
4������� ����Fe3+�� Ag  ?Fe2+ �� Ag+ ������Fe3+������Һ����ʴҺ���Թ��е�����ϴȥ��
?Fe2+ �� Ag+ ������Fe3+������Һ����ʴҺ���Թ��е�����ϴȥ��
��1��FeCl3��Һ�����ԣ�ԭ����?�������ӷ���ʽ��ʾ����
��2������FeCl3��Һϴ��������������ȷ����?������ţ���
a��c��Fe3+����С��������b��c��Cl-�����䡡����c����Ԫ��������С
��3��Fe(NO3)3��Һϴ��ʱ����ͬѧ��ΪNO3��Ҳ�ܽ�������������Ϊ����ͨ������Fe(NO3)3��Һϴ����NO3���Ļ�ԭ�������ж�NO3���Ƿ��ܽ�������������ͬѧ��Ϊ�˷�����?���У���ͬѧ��������?��
��4����ͬѧ����ϴ����Һ��Fe3+�� Fe2+�� Ag+�� NO3-���л������Ϳ�ʴҺ�����������·�ߣ�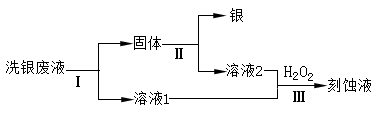
�ٹ��̢��з�Ӧ�����ӷ���ʽ��?��
�ڹ��̢��м�����Լ�������?��
��5���������������Һ����ʱ��������ǿ��ը�Ե����ʣ����Բ������档��������Һ�л������ķ����ǣ���������Һ�м���������ᣬ���ˣ������AgCl�м����ǰ���NH2OH������ַ�Ӧ��ɵ������ǰ�������ΪN2��
������AgCl�����Ļ�ѧ����ʽ��?��
�����÷�Ӧ������3.3 g�ǰ��������Ͽɵ���������Ϊ?g��
�ο��𰸣���1��Fe3����3H2O  ?Fe(OH)3��3H+?��2��a
?Fe(OH)3��3H+?��2��a
��3������������NO3��Ҳ������Fe2+����������ԭ��Ӧ?��4����2Fe3����Fe=3Fe2��?Fe��2Ag��=Fe2����2Ag
��ϡ�����ϡ����?��5����Ag(NH3)2OH��3HCl=AgCl����2NH4Cl��H2O?��10.8
�����������1��FeCl3��Һ����������Ϊ������ˮ���������������������ӣ���Ӧ�����ӷ���ʽΪ��Fe3++3H2O?Fe��OH��3+3H+����2��FeCl3��Һϴ����������ӦΪ��Fe3++Ag?Fe2++Ag+��a��c��Fe3+����С����a���ϣ�b�� c��Cl-�����䣬��b�����ϣ�c����Ԫ�ش�����ʽ��ͬ�����������С����c�����ϣ���3������ͨ������Fe��NO3��3��Һϴ����NO3-�Ļ�ԭ�������ж�NO3-�Ƿ��ܽ���������ͬʱע��������Һ�У���������Ҳ�ᷴӦ����4����ϴ����Һ��Fe3+��Fe2+��Ag+��NO3-���л������Ϳ�ʴҺ��Ҫ�ȼ������������ԭFe3+��Ag+����Ӧ�����ӷ���ʽΪ��2Fe3++Fe=3Fe2+Fe+2Ag+=Fe2++2Ag���ڹ��̢��м�����Լ����ܽ����������������ϡ�����ϡ�����5����������Һ�м���������������Ȼ�����ͬʱ�����Ȼ�狀�ˮ����Ӧ�Ļ�ѧ����ʽΪ��Ag��NH3��2OH+3HCl=AgCl��+2NH4Cl+H2O���������AgCl�м����ǰ���NH2OH������ַ�Ӧ��ɵ������ǰ�������ΪN2����ӦΪ��2AgCl+2NH2OH=N2��+2Ag+2H2O+2HCl����Ӧ������3.3g�ǰ����ʵ���= =0.1mol�������������ʵ���0.1mol������10.8g��
=0.1mol�������������ʵ���0.1mol������10.8g��
�����Ѷȣ�����
5��ѡ���� ���������ε�ϡ��Һ���ֱ���a mol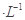 NaX��Һ��b mol
NaX��Һ��b mol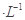 NaY��Һ������˵������ȷ����(? )��
NaY��Һ������˵������ȷ����(? )��
A����a=b��pH(NaX)>pH (NaY)������ͬŨ��ʱ������HX>HY
B����a=b�������c��X����="c" (Y��)+c(HY)������ͬŨ��ʱ������HX>HY
C����a>b�����c(X��)=c(Y��)������Ƴ���Һ��c(HX)>c(HY)������ͬŨ��ʱ�� ����HX<HY
D��������Һ�������ϣ����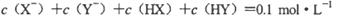
����Ƴ�a+b=0��2 mol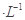
�ο��𰸣�A
���������A����a=b��pH(NaX)>pH (NaY)������Խ��Խˮ�����ͬŨ��ʱ������HX<HY,����B����a=b�������c��X����="c" (Y��)+c(HY)��˵��Y��ˮ��̶ȱ�X������Խ��Խˮ������ͬŨ��ʱ������HX>HY,��ȷ��C��a>b�����c(X��)=c(Y��)��˵��X��ˮ��̶ȱ�Y����������c(HX)>c(HY)������ͬŨ��ʱ�� ����HX<HY����ȷ��D������Һ�������ϣ�����a="2" [c(X��)+ c(HX) ],b="2" [c(Y��)+ c(HY) ],����a+b=2��0��1mol/L=0��2 mol/L����ȷ����ѡA��
�����Ѷȣ�һ��