时间:2020-08-23 08:05:37
1、选择题 等体积等浓度的MOH强碱溶液和HA弱酸溶液混合后,混合溶液中有关离子浓度的关系正确的是
A.c(M+)>c(OH-)>c(A-)>c(H+)
B.c(M+)>c(A-)>c(H+)>c(OH-)
C.c(M+)>c(A-)>c(OH-)>c(H+)
D.c(M+)+ c(H+) =c(A-)+ c(OH-)
2、填空题 海水制取溴:
(1)主要流程:
(2)主要反应(化学反应方程式):
_____________________________________。
(3)最后分离实验操作是 、
3、选择题 在C2H2、C6H6、C2H4O组成的混合物中,已知碳元素的质量分数为84%,则混合物中氧元素的质量分数是
A.9%
B.8%
C.7%
D.12%
4、填空题 (方程式每空2分,其余每空1分,共20分。)氧化还原反应和离子反应是高一所学过的重要化学反应类型,仔细思考回答下列问题:
(Ⅰ)下列一组有水参与的反应:
①2Na + 2H2O =" 2NaOH" + H2↑ ②2Na2O2 + 2H2O =" 4NaOH" + O2↑
③Na2O+ H2O =2NaOH ④3Fe+4H2O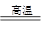 Fe3O4+4H2
Fe3O4+4H2
⑤2H2O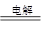 2H2↑+ O2↑ ⑥2F2 + 2H2O =" 4HF" + O2
2H2↑+ O2↑ ⑥2F2 + 2H2O =" 4HF" + O2
(1)其中不属于氧化还原反应的是 (填编号)
(2)在这些氧化还原反应中,水只作氧化剂的反应是 (填编号)
水只作还原剂的反应是 (填编号)
水既作氧化剂,又作还原剂是 (填编号)
水既不作氧化剂,又不作还原剂是 (填编号)
(3)根据你的理解,氧化还原反应的实质是( )
A.分子中的原子重新组合
B.氧元素的得失
C.电子的得失或共用电子对的偏移
D.化合价的改变
(4)请你运用所学知识分析3NO2+H2O = 2HNO3+NO是否属于氧化还原反应? (填“是”或“不是”),若是,这个反应的氧化剂和还原剂的质量比是 。
(Ⅱ)写出下列反应的离子方程式:
①铜片与稀硝酸的反应:
②过量二氧化碳通入澄清石灰水:
③往氯化铝溶液中加入过量的NaOH溶液:
(Ⅲ)写出下列反应的化学方程式:
①二氧化硫发生催化氧化反应:
②制漂白液的反应:
③雕刻花玻璃的反应:
5、选择题 组成中有氢氧根的盐叫做碱式盐,酸根中有氢元素的盐叫酸式盐(现阶段认为正确),下列盐中,既不是碱式盐又不是酸式盐的是
A.KHSO4
B.NH4NO3
C.Cu2(OH)2CO3
D.Ca(H2PO4)2[