时间:2020-08-23 06:57:47
1、选择题 下列分子的空间构型判断不 正确的是:
正确的是:
A.SO2角型
B.CCl4正四面体
C.SCl4正四面体
D.SCl6正八面体
2、选择题 下列叙述正确的是( )
A.乙醇的结构简式为:C2H6O
B.硫离子的结构示意图为: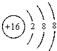
C.NaHCO3电离:NaHCO3=Na++H++CO32-
D.H2O的电子式: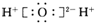
3、填空题 (6分)干冰和二氧化硅晶体同属ⅣA元素的最高价氧化物,它们的熔沸点差别很大的原因是?;氨易溶于水的原因是?(写出两点即可)
4、填空题 (12分)已知:A、B、C、D、E为周期表1~36号中的元素,它们的原子序数逐渐增大。A的基态原子有3个不同的能级,各能级中电子数相等;C的基态原子2p能级上的未成对电子数与A原子相同;C2―离子D2+离子具有相同的、稳定的电子层结构;E的基态原子的外围电子排布式为3d84s2。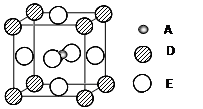
 请回答下列问题:
请回答下列问题:
⑴A、B、C、D四种元素中,电负性最大的是?▲?(填元素符号)。
⑵B的氢化物的沸点远高于A的氢化物的主要原因是?▲?。
⑶由A、B、C形成的离子CAB-与AC2互为等电子体,则CAB-中A原子的杂化方式为?▲?。
⑷E2+离子能与AC分子形成[E(AC)4]2+,其原因是AC分子中含有?▲?。
⑸最近发现,只含A、D、E三种元素的一种晶体(晶胞如右图所示)具有超导性。A原子的配位数为?▲?;该晶体的化学式为?▲?。
5、选择题 下列物质变化过程中有共价键明显被破坏的是
[? ]
A.I2升华
B.NaCl颗粒被粉碎
C.HCl溶于水得盐酸
D.从NH4HCO3中闻到了刺激性气味