ʱ��:2020-08-23 06:55:18
1������� (10��)�����£���100mL0.01mol��L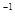 HA��Һ����μ���0��02mol
HA��Һ����μ���0��02mol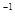 MOH��Һ��ͼ����ʾ���߱�ʾ�����Һ��pH�仯�������仯���Բ���)
MOH��Һ��ͼ����ʾ���߱�ʾ�����Һ��pH�仯�������仯���Բ���) ���ش��������⣺
���ش��������⣺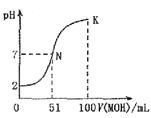
(1)��ͼ����Ϣ��֪HAΪ ��(�ǿ���� ���������������� ��
(2)������һ��Ũ�ȵ�MAϡ��Һ��pH=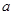 ����
����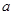 7(�>������<����=��)�������ӷ���ʽ��ʾ��ԭ��Ϊ ����ʱ����Һ����ˮ�������c(OH
7(�>������<����=��)�������ӷ���ʽ��ʾ��ԭ��Ϊ ����ʱ����Һ����ˮ�������c(OH )= ��
)= ��
(3)��д��K������Ӧ����Һ������Ũ�ȵĴ�С��ϵ�� ��
(4)K���Ӧ����Һ�У�c(M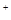 )+c(MOH) 2c(A
)+c(MOH) 2c(A )(�>������<����=��)������ʱ��Һ�У�pH=lO����c(MOH)+c(OH
)(�>������<����=��)������ʱ��Һ�У�pH=lO����c(MOH)+c(OH )= mol��L
)= mol��L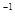 ��(�ô���ʽ��ʾ)
��(�ô���ʽ��ʾ)
�ο��𰸣�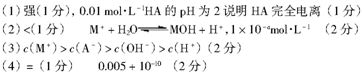
�����������
�����Ѷȣ�һ��
2��ѡ���� ���е��뷽��ʽ�У���ȷ���ǣ�������
A��Al2��SO4��3�T2Al+3+3SO4-2
B��Na2CO3�TNa2++CO32-
C��NaOH�TNa++OH-
D��NaHCO3�TNa++H++CO32-
�ο��𰸣�A�����ʵ����DZ�Ҫת���ɻ�ѧ��������ͬʱע�����������ĵ��������ȷ�����ӷ���ʽΪ��Al2��SO4��3�T2Al3++3SO42-����A����
B����ȷ�����ӷ���ʽΪ��Na2CO3�T2Na++CO32����B����
C������������ǿ���ˮ��Һ����ȫ����������Ӻ����������ӣ���C��ȷ��
D��̼����������ȫ����������Ӻ�̼��������ӣ�̼�����������һ�����壬�����ٲ�NaHCO3�TNa++HCO3-����D����
��ѡC��
���������
�����Ѷȣ�һ��
3������� ��3�֣����ʵ���Ũ�Ⱦ�Ϊ0.1mol/L��������Һ����KNO3 ����Na2CO3 ����NaHCO3 ����NaHSO4 ����CH3COOH����NaOH����Ba(OH)2 ��pH�ɴ�С��˳��Ϊ�� ��
�ο��𰸣���3�֣����ߢޢڢۢ٢ݢ�
����������������ǿ��ǿ���Σ���Һ�����ԣ�̼������ǿ�������Σ�ˮ���Լ��ԣ�̼��������Һ��ˮ��̶ȴ��ڵ���̶ȣ����������Լ��ԣ�����������ǿ�����ʽ�Σ���Һ��ǿ���ԣ����������ᣬ��Һ�����ԣ�����������ǿ���Һ�Լ��ԣ����������Ƕ�Ԫǿ���Һ�Լ��ԣ�����pH�ɴ�С��˳��Ϊ�ߢޢڢۢ٢ݢܡ�
���㣺������Һ�����ǿ���жϡ�
���������ж���Һ�������ʱӦ��ȷ�жϵ���ʵ�ǿ���Լ������Ƿ�ˮ��ȡ�
�����Ѷȣ�һ��
4��ѡ���� �����£�����pH = 11��NaOH��Һ������˵���������
A��c(OH��) =c(Na+) + c(H+)
B������Һ�е�c(OH��) = 1��0��10-3 mol��L-1
C��������pH = 3�Ĵ����Ϻ�������Һ�Լ���
D��������0��001 mol��L-1���Ȼ�炙�Ϻ�������Һ�У�c(Na+)>c(NH4+)
�ο��𰸣�C
���������A�����ݵ���غ�ɵ�c(OH��) =c(Na+) + c(H+)����ȷ��B�� pH = 11��NaOH��Һ, c(H+)= 1��0�� 10-11mol/L ��������������ˮ�����ӻ��Ǹ����������Ը���Һ�е�c(OH��) = 1��0��10-3 mol��L-1����ȷ��C��NaOH��ǿ���ȫ���룬���������ᣬ���ֵ��룬��������pH = 3�Ĵ����Ϻ����������������������Һ�����ԣ�����D��������0��001 mol��L-1���Ȼ�炙�Ϻ�������Һ�������Ե�Ũ�ȵ�NaCl��NH3?H2O,����һˮ�ϰ���������ֵ��룬����Һ�д��ڵ���ƽ�⣬����c(Na+)>c(NH4+)����ȷ��
���㣺������Һ������Ũ�ȴ�С�Ƚϡ���Һ����Ե��жϵ�֪ʶ��
�����Ѷȣ�һ��
5��ʵ���� ��14�֣�ij������ȤС�����ⶨijNaOH��Һ��Ũ�ȣ�������������£�
�ٽ���ʽ�ζ���������ˮϴ������鲻©ˮ�����ô�����Һ��ϴ����ע�������Һ�����ڵζ��ܵļ��첿�ֳ�����Һ����ʹҺ�洦�ڡ�0���̶����µ�λ�ã����¶���������ƿ������ˮϴ�����ô�����Һ��ϴ��ƿ2��3�Σ��Ӽ�ʽ�ζ����з���25��00 mL������Һ����ƿ�С�
�ڽ���ʽ�ζ���������ˮϴ������鲻©ˮ������������ע��0��1000 mol/L�����ᣬ���ڵζ��ܵļ��첿�ֳ�����Һ����ʹҺ�洦�ڡ�0���̶����µ�λ�ã����¶�����
������ƿ�е����̪��ָʾ�������еζ����ζ���ָʾ���պñ�ɫ������30 s����ɫ���ٱ仯�����������������ΪV1 mL��
���ظ����Ϲ��̣����ڵζ�����������ƿ�м���5 mL������ˮ�����������������ΪV2 mL��
�Իش��������⣺
��1����ƿ�е���Һ��_____ɫ��Ϊ_____ɫʱ��ֹͣ�ζ���
��2���ζ�ʱ�ߵα�ҡ����ƿ���۾�Ӧ�۲�_____��
A���ζ�����Һ��ı仯 B����ƿ����Һ��ɫ�ı仯
��3����С���ڲ�����еĴ�����__________���ɴ���ɵIJⶨ���_____(�ƫ�ߡ�����ƫ�͡�����Ӱ�족)
��4�������ȱ�ٵIJ�����__________��
��5����ͼ����ij�εζ�ʱ�ĵζ����е�Һ�棬�����Ϊ_____ mL��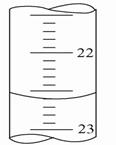
�ο��𰸣��ź죨2�֣� dz�죨��ۺ죩��2�֣���B (2�֣����ô���Һ��ϴ��ƿ��2�֣� ƫ�ߣ�2�֣�
���ñ�Һ��ϴ�ζ��ܣ�2�֣���22��60��22��59Ҳ�ɣ���2�֣�
�����������1����Һ�Ӽ�����Ϊ���Թ�������Һ��ɫ�仯��Ϊ���Ӻ�ɫ��Ϊdz��ɫ����2���ζ��������۾�Ҫע����ƿ�е���Һ��ɫ�仯����3�����������д�����ǣ��ô���Һ��ϴ��ƿ������ô���Һ��ϴ��ƿ������ɴ���Һ���࣬������������������Ũ��ƫ�ߡ���4���ζ�ǰҪ���ñ�Һ��ϴ�ζ��ܣ��������ɱ�ҺŨ�ȱ�С��������Ĵ���ҺŨ��ƫ�ߡ���5����ͼ�����ζ���ÿһС����0��1 mL��Һ��պ���6�����У�����Ҫ����С�����2Ϊ���ʶ���Ϊ22��60 mL
���㣺����к͵ζ���
�����Ѷȣ�һ��