ʱ��:2020-08-23 06:50:43
1��ѡ���� ͼ�����Ǽĵ��ؽ��е��ʱ��ij����(������x)��ʱ��仯������(�����ض���ʯī���缫�������ǵ���������ҺŨ�ȱ仯�Ե缫��Ӧ��Ӱ��)����x��ʾ(? )
A������������������������ı仯
B����������������������
C����������������������
D�����缫�Ϸŵ�����������ı仯
�ο��𰸣�C
��������������ŵ��Ľ���xֵʼ��Ϊ0�����ų�A��������ص������϶��������ӷŵ磬���Т٢��������Ķ���������������ͬ���ʿ��ų�B����缫�Ϸŵ�����������٢�����ͬ�ģ�����D��Ҳ����ȷ
�����Ѷȣ�һ��
2��ѡ���� �ò����缫���һ��Ũ�ȵ��������ʵ�ˮ��Һ������������ʣ����Һ�м�����ˮ������ʹ��Һ�͵��ǰ��ͬ���ǣ�������
A��AgNO3
B��H2SO4
C��NaOH
D��NaNO3
�ο��𰸣�A����⣬��������Ag������������������ʣ����Һ�м�����ˮ������ʹ��Һ�͵��ǰ��ͬ����Aѡ��
B�����H2SO4���������ɵIJ������������������൱�ڵ���ˮ������ˮ��ʹ��Һ�͵��ǰ��ͬ����B��ѡ��
C�����NaOH���������ɵIJ������������������൱�ڵ���ˮ������ˮ��ʹ��Һ�͵��ǰ��ͬ����C��ѡ��
D�����NaNO3���������ɵIJ������������������൱�ڵ���ˮ������ˮ��ʹ��Һ�͵��ǰ��ͬ����D��ѡ��
��ѡA��
���������
�����Ѷȣ���
3������� �ڰ���ͼװ�ý��е��Ĺ����У�ͨ��һ��ʱ��������ձ������缫���������ӡ� 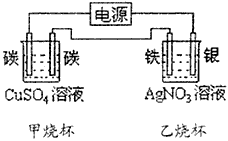
��1�����ձ��У����������ĵ缫��Ӧ��
������_____________________������______________________
��2�����ձ��з�����Ӧ�Ļ�ѧ����ʽ�ǣ�_____________________
��3��������̼-̼-��-���ĸ��Ǽ����������ܽ����ʵ����ʵ���֮����_____________________��
�ο��𰸣���1��������Ag++e-=Ag��������Ag-e-=Ag+
��2��2CuSO4+2H2O 2Cu+O2��+2H2SO4
2Cu+O2��+2H2SO4
��3��2 ��1 ��4 ��4
���������
�����Ѷȣ�һ��
4��ѡ���� ��ҵ�ϵ�ⱥ��ʳ������ȡ���ֻ���ԭ�ϣ���ͼ�����ӽ���Ĥ����ⱥ��ʳ��ˮʾ��ͼ������˵���в���ȷ���ǣ�������
A�����������ķ�Ӧ����ʽΪ��2Cl--2e-�TCl2��
B����Ʒ?NaOH�ij�����b
C�����Ʊ���ʳ��ˮ�Ľ���Ϊd
D����������Ӧʹ�õ�Һ����Ũ����
�ο��𰸣�A������ͼװ�ÿ�֪�����������������ӷŵ������������缫��ӦΪ��2Cl--2e-�TCl2������A��ȷ��
B�������������������ӷŵ�����������ˮ����ƽ�������������������Ũ��������������������Һ��NaOH��Һ�ij���Ϊa����B����
C��Cl2������������װ��ͼ������֪���Ʊ���ʳ��ˮ���������룬������Ϊd����C��ȷ��
D��Ҫ����Cl2��Ҫ�����Ը���������Ը������������Ũ��������D��ȷ��
��ѡB��
���������
�����Ѷȣ���
5��ѡ���� �ö��Ե缫���CuSO4��Һһ��ʱ���ֹͣ��⣬��������Һ�м���0.1 mol Cu(OH)2����ҺŨ�Ȼָ������ǰ�����ڸõ����̵�˵������ȷ����
A������Cu�����ʵ�����0.1 mol
B��ת�Ƶ��ӵ����ʵ�����0.2 mol
C�����ŵ��Ľ�����Һ��pH��С
D��������Ӧʽ��4OH-��4e-��2H2O��O2��
�ο��𰸣�B
�������������0.1 mol Cu(OH)2����ҺŨ�Ȼָ������ǰ��˵�����CuSO4��Һ�������H2SO4��Һ��A������CuԪ���غ㣬����Cu�����ʵ�����0.1 mol����ȷ��B������0.1 mol Cu(OH)2����ҺŨ�Ȼָ������ǰ��˵�������0.1mol��CuSO4��0.1mol��H2O��ת�Ƶ��ӵ����ʵ���Ϊ0.4mol������C�����CuSO4��Һʱ����H2SO4�����H2SO4��Һ��ʵ�ʵ��ˮ��H2SO4Ũ������pH��С����ȷ��D�����CuSO4��Һ��H2SO4��Һ��������Ӧ���ǣ�4OH-��4e-��2H2O��O2������ȷ��
�����Ѷȣ�һ��