时间:2020-08-23 06:47:33
1、选择题 有Fe2+、NO—3、Fe3+、NH+4、H2O和H+六种微粒,分别属于一个氧化还原反应中的反应物和生成物,下列叙述错误的是( )
A.氧化剂与还原剂的物质的量之比为8:l
B.若有l mol NO—3参加还原反应,则转移8mol e-
C.还原产物为NH+4
D.若把该反应设计为原电池,则负极反应为Fe2+—e—=Fe3+
2、填空题 (4分) 实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下
2KMnO4+16HCl(浓) = 2KCl+2MnCl2+5Cl2↑+8H2O
(1)在该反应中,还原剂是 。
(2)若在反应中生成了标况下2.24L氯气,则电子转移的个数是 NA。
3、填空题 有4种钠的化合物W、X、Y、Z,它们之间存在如下关系:
①W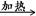 X+H2O+CO2↑
X+H2O+CO2↑
②Z+CO2
4、选择题 下列过程是自发进行的吸热反应的使
A.NaOH与HCl 反应
B.CO与O2点燃
C.Ba(OH)2·8H2O与NH4NO3反应
D.SO3与H2O反应
5、选择题 分子式为C5H12O的一元醇有多种同分异构体,其中主链上碳原子数为3的同分异构体数目为m,主链上碳原子数目为4的同分异构体数目为n。下列关于m、n的数值正确的是
A.m=1 n=4
B.m=1 n=5
C.m=2 n=5
D.m=2 n=5