时间:2020-08-23 06:42:19
1、选择题 a、b的活动性均比氢强,a还可以从b的硝酸盐中置换出b。将a、b用导线相连放入CuSO4溶液中,下列叙述中不正确的是
[? ]
A.导线上有电流,电流方向由a到b
B.a极质量减少,b极质量增加
C.b棒上析出氢气
D.a棒发生氧化反应,b棒发生还原反应
参考答案:A
本题解析:
本题难度:一般
2、选择题 某化学兴趣小组将锌片和铜片出入番茄中制成水果电池(如图)( )
A.一段时间后,锌片质量会变小
B.铜片上发生氧化反应
C.电子由铜片通过导线流向锌
D.锌电极是该电池的正极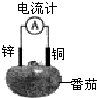
参考答案:A、锌在原电池中做负极失电子溶解,锌片质量会变小,故A正确;
B、铜做正极发生还原反应,故B错误;
C、原电池中电子从负极流出沿导线到正极,即从锌流向铜,故C错误;
D、锌电极是该电池的负极,故D错误;
故选A.
本题解析:
本题难度:一般
3、选择题 实验室欲快速制取氢气,最好的方法应该用
A.纯锌与稀H2SO4反应
B.纯锌与浓H2SO4反应
C.粗锌与硝酸反应
D.粗锌(含Pb、Cu等杂质)与稀H2SO4反应
参考答案:D
本题解析:本题考查的是对反应速率的影响因素.影响化学反应速率的外界因素主要有:浓度、温度、压强、催化剂、接触面积等.此外若形成原电池则可加快反应速率.本题中A为正常反应,B、C发生反应时,因浓H2SO4和硝酸为氧化性酸,故不会产生H2.D中Pb、Cu与Zn可形成原电池,故制取氢气的速率可加快.
本题难度:一般
4、填空题 Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlClx-SOCl2。电池的总反应可表示为:4Li+2SOCl2=4LiCl+S+SO2↑。请回答下列问题:
(1)电池的负极材料为 ,发生的电极反应为 。
(2)电池正极发生的电极反应为 。
(3)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成。如果把少量水滴到SOCl2中,实验现象是 ,反应的化学方程式为 。
(4)组装该电池必须在无水、无氧的条件下进行,原因是 。
参考答案:(1)锂 Li- e-= Li+
(2)2SOCl2+4e-=4Cl-+S+SO2↑
(3)出现白雾,有刺激性气体生成SOCl2+H2O=SO2↑+2HCl↑
(4)锂是活泼金属,易与H2O、O2反应;SOCl2也可与水反应
本题解析:分析反应的化合价变化,可得Li为还原剂,发生氧化反应,SOCl2为氧化剂,发生还原反应。(1)负极材料为Li(还原剂),Li- e-=Li+。
(2)正极反应式可由总反应减去负极反应式得到:2SOCl2+4e-=4Cl-+S+SO2↑
(3)题中给出有碱液吸收时的产物,则没有碱液吸收时的产物应为SO2和HCl,所以现象应该为出现白雾和有刺激性气体生成。
(4)因为构成电池的两个主要成份Li能和氧气水反应,且SOCl2也与水反应。所以组装该电池必须在无水、无氧的条件下进行。
考点:考查原电池反应原理的应用,电池正负极的判断,电极反应式的书写,现象的判断
本题难度:一般
5、选择题 锰锌干电池在放电时,电池总反应方程式可以表示为:Zn+2MnO2+2NH4+=Zn2++Mn2O3+2NH3+H2O.在此电池放电时,正极(碳棒)上发生反应的物质是( )
A.Zn
B.碳
C.MnO2和NH4+
D.Zn和NH3
参考答案:锰锌干电池在放电时,发生Zn+2MnO2+2NH4+=Zn2++Mn2O3+2NH3+H2O,
Zn元素的化合价升高,失去电子,作负极,
则正极(碳棒)上,Mn元素的化合价降低,所以MnO2得到电子发生还原反应,只有C符合,
故选C.
本题解析:
本题难度:一般