ʱ��:2020-08-23 06:29:05
1��ѡ���� ���й�����Һ�����ӵ�˵����ȷ����?
A��0.1mol��L-1��Na2CO3��Һ������Ũ�ȹ�ϵ��c(Na+)=2 c(CO )+ c(HCO
)+ c(HCO )+ c(H2CO3)
)+ c(H2CO3)
B��0.1mol��L-1��NH4Cl��0.1mol��L-1��NH3��H2O�������Ϻ���Һ�е�����Ũ�ȹ�ϵ��
c(Cl��)> c(NH )> c(OH��)> c(H+)
)> c(OH��)> c(H+)
C�������£���������Һ�еμ���������ʹ��Һ��pH=7��������Һ�У�����Ũ�ȹ�ϵ��
c(Na+)< c(CH3COO��)
D�������ʵ���Ũ�ȡ��������NH4NO3��KNO3��Һ�У�ǰ�ߵ�������Ũ��С�ں��ߵ�������Ũ��
�ο��𰸣�D
�����������
�����Ѷȣ���
2��ѡ���� ��һ��������Na2CO3��Һ����ˮ��ƽ�⣺CO32++H2O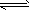 HCO3-+OH-������˵����ȷ����
HCO3-+OH-������˵����ȷ����
[? ]
A��Na2CO3��Һ�У�c(Na+)>c(CO32-)>c(OH-)>c(H+)
B�������¶ȣ�ƽ��������Ӧ�����ƶ�
C��ϡ����Һ����Һ��c(H+)��c(OH-)������
D������NaOH���壬��ҺpH��С
�ο��𰸣�AB
���������
�����Ѷȣ�һ��
3������� ���������£�����ˮ��Һ����Sn2+��Sn4+������Ҫ������ʽ��SnSO4��һ����Ҫ�������Σ��㷺Ӧ���ڶ�����ҵ�����Ʊ�·�����£�
�ش��������⣺
��1��SnCl2�����������ˮֱ���ܽ��ԭ����?
�������۵�������?
��2����ӦI���ɵij���ΪSnO��д���÷�Ӧ�Ļ�ѧ����ʽ��?
��3����������Ѿ���ϴ�ӡ��ɾ��IJ����ǣ�?��3�֣�
��4����Ӧ�����������֮һ�ǿ�����Һ��pH������Һ��c(Sn2+)=1.0mol��L��1����������Ӧ������ҺpH?������֪��Ksp[Sn(OH)2]=1.0��10��26��
��5�����������£�SnSO4��������˫��ˮ��ȥ��������д����������Ӧ�����ӷ���ʽ��
?��
��6����ʪ�����У�����ͭ��ʹ��������Ҳ�ܷ�ֹ�γ�ͭ�̣������йص�ԭ��������ԭ��
?��
�ο��𰸣���1������Sn2+ˮ�⣬?��ֹSn2+������ ��2��SnCl2 + Na2CO3 =" SnO" + CO2��+2NaCl��3��ȡ�������һ��ϴ��Һ���Թ��У����뼸��AgNO3��Һ�����ް�ɫ�������ɣ���˵��������ϴ�Ӹɾ���3�֣���4��С��1?��2�֡���д�ɡ�1��1�֣� ��5��Sn2+ + H2O2 + 2H+ = Sn4+ + 2H2O ��6����ʪ�����У�Sn��Cu����ԭ��أ�Sn��Ϊ��������������Cu��������
�����������1��SnCl2��ˮ�����ɼ�ʽ�Ȼ�����������ƽ��Sn Cl2+H2O?Sn��OH��Cl+HCl���������ᣬʹ��ƽ�������ƶ�������Sn2+ˮ�⣻Sn2+�ױ�����������Sn�۳�������ҺpH�⣬����ֹSn2+����������2����Ӧ��õ�������SnO��SnԪ�ػ��ϼ�Ϊ�仯�����ڷ�������ԭ��Ӧ��ͬʱ�������壬������Ϊ������̼�����ӷ���ʽΪ��Sn2++CO32-�TSnO��+CO2������3����������Ѿ���Ưϴ���ɾ��ķ����ǣ�ȡ���һ��ϴ��Һ�������м���AgNO3��Һ������������˵��ϴ�Ӹɾ�����4������ Ksp[Sn��OH��2]=1.0��10-26=c��OH-��2��c��Sn2+������c��Sn2+��=1.0mol?L-1���˿ɵ�c��OH-��=10-13mol/L��c��H+��=0.1mol/L����PHС��1��Sn2+��ȫ��������5�����������£�SnSO4����������˫��ˮȥ������˫��ˮ��ǿ�����ԣ���Sn2+�ױ�����ΪSn4+����������ԭΪˮ�����ӷ���ʽΪ��Sn2++H2O2+2H+�TSn4++2H2O����6����ʪ�����У�Sn��Cu����ԭ��أ�Sn��Ϊ��������������Cu����������
�����Ѷȣ�һ��
4��ѡ���� ���е����ʵ�����CH3COOH��CH3COONa�Ļ����Һ�У�����˵����ȷ����
A��c(CH3COOH) + c(H+ )��c(OH��) + c(CH3COO��)
B��c(H+ ) + c(CH3COOH) = c(OH��) + c(CH3COO��)
C��c(Na+)��c(CH3COO��)��c(OH��)��c(H+)
D��c(Na+) = c(CH3COOH) + c(CH3COO��)
�ο��𰸣�A
������������е����ʵ�����CH3COOH��CH3COONa�Ļ����Һ�У�����ĵ���̶ȴ���CH3COO����ˮ��̶ȣ���Һ�����ԣ�����ѡ��C����ȷ�����ݵ���غ��֪c(H+ ) + c(Na+)�� c(OH��) + c(CH3COO��)������c(Na+)��c(CH3COOH)����c(CH3COOH) + c(H+ )��c(OH��) + c(CH3COO��)��A��ȷ��B����ȷ�����������غ��֪��2c(Na+)��c(CH3COOH) + c(CH3COO��)��D����ȷ����ѡA��
�����������Ǹ߿��еij������ͣ������е��Ѷ�����Ŀ��顣����Ĺؼ��ǵó���Һ�����ԣ�Ȼ�������úõ���غ㡢�����غ��Լ������غ㼴�ɡ���Щ�غ㷨����ʱ��Ҫע�������ܽᡣ
�����Ѷȣ�һ��
5��ѡ���� ���й�������ˮ�ⷴӦ˵����ȷ����
A���κ��ζ��ɷ���ˮ�ⷴӦ
B����ֻ�ܷ���ˮ�ⷴӦ�����ܷ���������Ӧ
C����ˮ�ⷴӦ�϶����ƻ�ˮ�ĵ���ƽ���Ҵٽ�ˮ�ĵ���
D���ε�ˮ��ҺΪ����ʱ������һ��������ˮ�ⷴӦ
�ο��𰸣�C
���������
��ȷ�𰸣�C
A������ȷ��������������γɵ��βſɷ���ˮ�ⷴӦ
B������ȷ��ˮ��ֻ��ijЩ�ε����ʣ�
C����ȷ����ˮ�ⷴӦ�϶����ƻ�ˮ�ĵ���ƽ���Ҵٽ�ˮ�ĵ���?
D������ȷ���ε�ˮ��ҺΪ����ʱ�������ֿ��ܣ�һ��ǿ��ǿ���β�����ˮ�ⷴӦ���������������Σ�ˮ��������ࡣ
�����Ѷȣ���