时间:2020-08-23 06:09:15
1、选择题 下列变化属于吸热反应的是
①碳与二氧化碳化合
②生石灰与水反应生成熟石灰
③Zn与稀硫酸反应
④氯酸钾分解制氧气
⑤Ba(OH)2.8H2O与NH4Cl反应
⑥甲烷与氧气的燃烧
A.①④
B.②③
C.①④⑤
D.①②④
2、填空题 )根据下图所示的能量变化,写出下列反应的热化学方程式并回答相关问题:
(1)____________________________________________________________________;
(2)____________________________________________________________________。
Q1与Q2的关系:Q1____________(填“大于”“小于”或“等于”)Q2。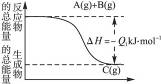
反应过程(1)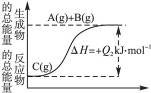
反应过程(2)
3、填空题 能源短缺是人类社会面临的重大问题,世界各国都在努力寻找新能源,探求绿色能源的开发。甲醇是一种可再生能源,是一种污染性较小,热值较大的能源,因而具有广泛的开发价值和良好的应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应I: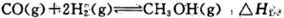
反应Ⅱ: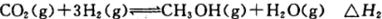
①上述反应符合“原子经济”原则的是_________(填“I’’或“Ⅱ”)。
②下表所列数据是反应I在不同温度下的化学平衡常数(K)
由表中数据判断△H1_________0(填“>”、“=”或“<”),说明生成物的总能量一定_______(填“>”、“=”或“<”)反应物的总能量。
③反应Ⅱ反应历程如下图,回答下列问题;在反应体系中加入催化剂,反应速率增大,E1、E2和△H2的变化是:E1_________、E2_________、△H2_________(填“增大”“减小”“不变”)。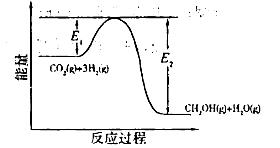
(2)最新研制的一种新型甲醇电池示意图如图,电池的两极分别充人甲醇和氧气(池内为酸性介质)。则电池工作时____________(填a或b)为正极,a极的电极反应式为______________。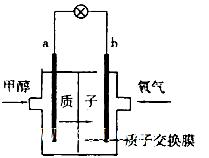
4、选择题 25 ℃,101 k Pa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ/mol,辛烷的燃烧热为5518 kJ/mol。下列热化学方程式书写正确的是( )
A.2H+(aq) + (aq)+
(aq)+ (aq)+2OH
(aq)+2OH (aq)=BaSO4(s)+2H
(aq)=BaSO4(s)+2H O(l);
O(l); H=
H= 57.3 kJ/mol
57.3 kJ/mol
B.KOH(aq)+ H
H SO4(aq)=
SO4(aq)=  K
K SO4(aq)+H
SO4(aq)+H O(l);
O(l); H=
H= 57.3kJ/mol
57.3kJ/mol
C.C8H18(l)+  O
O (g)=8CO
(g)=8CO (g)+ 9H
(g)+ 9H O;
O; H=
H= 5518 kJ/mol
5518 kJ/mol
D.2C8H18(g)+25O (g)=16CO
(g)=16CO (g)+18H
(g)+18H O(l);
O(l); H=
H= 5518 kJ/mol
5518 kJ/mol
5、选择题 二氧化硫是引起酸雨的一种物质.?二氧化硫属于
A.酸
B.酸性氧化物
C.碱
D.混合物