时间:2020-08-13 07:28:00
1、选择题 如图所示,在用锌片、铜片和稀硫酸组成的原电池装置中,下列说法正确的是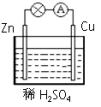
A.铜电极上的反应为Cu-2e-==Cu2+
B.锌电极上的反应为2H++2e-==H2↑
C.锌片是负极,铜片是正极
D.电子由铜片经导线流向锌片
参考答案:C
本题解析:在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应。锌比铜活泼,所以锌是负极,失去电子,铜是正极,溶液中的氢离子得到电子,所以答案选C。
本题难度:一般
2、选择题 下列叙述正确的是( )
A.构成原电池正极和负极的材料必须是两种金属
B.由Cu、Zn作电极与CuSO4溶液组成的原电池中Cu是负极
C.马口铁(镀锡铁)破损时与电解质溶液接触,锡先被腐蚀
D.铜锌原电池工作时,若有13g锌被溶解,电路中就有0.4mol电子通过
参考答案:A.构成原电池正负极的材料不一定是两种金属,可能是金属和非金属,如:锌、石墨、稀硫酸原电池,故A错误;
B.锌、铜和硫酸铜溶液构成的原电池中,锌易失电子作负极,铜作正极,故B错误;
C.锡、铁和电解质溶液构成的原电池中,铁易失电子作负极,锡作正极,所以铁易被腐蚀,故C错误;
D.铜锌原电池放电时,负极上电极反应式为Zn-2e-=Zn2+,根据锌和转移电子之间的关系式,当有13g锌被溶解,转移电子的物质的量=13g65g/mol×2=0.4mol,故D正确;
故选D.
本题解析:
本题难度:一般
3、选择题 某同学欲完成2HCl+2Ag═2AgCl↓+H2↑反应,设计了下列四个实验,你认为可行的实验是( )
A.
B.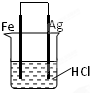
C.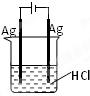
D.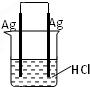
参考答案:C
本题解析:
本题难度:一般
4、选择题 下列说法正确的是
[? ]
A.原电池是把电能转化为化学能的装置
B.原电池中电子流出的是正极发生氧化反应
C.原电池两极发生的均为氧化还原反应
D.形成原电池后,阳离子向正极移动
参考答案:D
本题解析:
本题难度:简单
5、填空题 (13分)(1)将锌、铜用导线连接后浸入2mol/L的稀硫酸中,正极电极反应式为_________________,发生 反应(填氧化或还原);电子从 经外电路到 (填锌或铜),溶液中H+ 向 移动(填正极或负极)。
(2)根据反应2Fe3+ + Cu = 2Fe2++Cu2+ 设计原电池,所需负极材料为 ,溶液中Fe3+向 (填“负极”或“正极”)迁移,负极反应式为 ;正极反应式为 。
参考答案:(1)2H++2e-=H2↑ 还原 锌 铜 正极
(2)Cu、正、 Cu-2e-=Cu2+ 2Fe3+ +2e- = 2Fe2+
本题解析:(1)将锌、铜用导线连接后浸入2mol/L的稀硫酸中形成原电池,该原电池中锌是负极,发生氧化反应,铜是正极,溶液中的氢离子得电子生成氢气,发生还原反应,电极反应式为2H++2e-=H2↑;外电路上,电子从负极沿导线到正极,即电子是从锌经外电路到铜;溶液中H+ 向正极移动。(2)根据反应2Fe3+ + Cu = 2Fe2++Cu2+ 设计原电池,铜的化合价由0价升高为+2价,发生氧化反应,作原电池的负极,电极反应式为Cu-2e-=Cu2+;电解质溶液中阳离子Fe3+向正极迁移,在正极上发生还原反应,电极反应式为2Fe3+ +2e- = 2Fe2+。
考点:考查原电池原理、电极方程式书写。
本题难度:一般