时间:2020-08-13 07:24:29
1、选择题 下列判断正确的是( )
①稳定性:HI>HBr>HCl?②熔点:SiO2>NaCl>SiI4
③酸性:HClO4>H2SO4>H3PO4?④碱性:NaOH>Mg(OH)2>Al(OH)3
A.只有①
B.只有③
C.②③④
D.①②③④都正确
2、填空题 (8分)下表由元素周期表的前三周期去掉副族上方的空白区域后组合而成,表中虚线处为ⅡA、ⅢA族的连接处,请用相应的化学用语或符号回答下列问题:
| a | ? | ? | ? | ? | ? | ? | ? |
| b | ? | ? | c | d | e | f | ? |
| g | ? | h | ? | ? | ? | ? | ? |

3、选择题 浊液区别于其他分散系最本质的特征是
A.外观混浊不清
B.分散质粒子不能透过半透膜
C.不稳定
D.分散质粒子直径大于100 nm
4、填空题 [物质结构与性质]
含有NaOH的Cu(OH)2悬浊液可用于检验醛基,也可用于和葡萄糖反应制备纳米Cu2O。
(1)Cu+基态核外电子排布式为?
(2)与OH-互为等电子体的一种分子为?(填化学式)。
(3)醛基中碳原子的轨道杂化类型是?;1mol乙醛分子中含有ó的键的数目为?。
(4)含有NaOH的Cu(OH)2悬浊液与乙醛反应的化学方程式为?。
(5)Cu2O在稀硫酸中生成Cu和CuSO4。铜晶胞结构如图所示,铜晶体中每个铜原子周围距离最近的铜原子数目为?。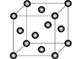
5、填空题 (14分)下表是周期表中的一部分,根据a―n在周期表中的位置,按要求回答问题:
| ? | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | a | ? | ? | |||||
| 2 | ? | ? | ? | b | c | ? | d | e |
| 3 | f | g | h | i | j | k | m | n |