ʱ��:2020-08-13 07:06:18
1��ѡ���� ��֪��Һ�д���Cr2O72-�� H2O 2CrO42-�� 2H+��ƽ�⣬����Cr2O72-�ʳ�ɫ��CrO42-�ʻ�ɫ�����ƽ����ϵ�еμӱ���NaOH��Һʱ����ɫ�ı仯�����
2CrO42-�� 2H+��ƽ�⣬����Cr2O72-�ʳ�ɫ��CrO42-�ʻ�ɫ�����ƽ����ϵ�еμӱ���NaOH��Һʱ����ɫ�ı仯�����
A����ɫ����
B����ɫ����
C����ɫ����
D����ɫ��ȥ
�ο��𰸣�A
���������
Cr2O72-�� H2O 2CrO42-�� 2H+�����ƽ����ϵ�еμӱ���NaOH��Һʱ��H��Ũ�ȼ�С��ƽ�������ƶ�����ɫ���A��ȷ��
2CrO42-�� 2H+�����ƽ����ϵ�еμӱ���NaOH��Һʱ��H��Ũ�ȼ�С��ƽ�������ƶ�����ɫ���A��ȷ��
�����Ѷȣ���
2��ѡ���� һ�������£������Ϊ10L���ܱ������У�1mol X��1mol Y���з�Ӧ��2X(g)��Y(g)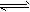 Z(g)����60s�ﵽƽ�⣬����0��3mol Z������˵����ȷ����
Z(g)����60s�ﵽƽ�⣬����0��3mol Z������˵����ȷ����
[? ]
A����XŨ�ȱ仯��ʾ�ķ�Ӧ����Ϊ0��001 mol/(L��s)
B�������������Ϊ20 L��Z��ƽ��Ũ�ȱ�Ϊԭ����1/2
C��������ѹǿ��������Y��ת���ʼ�С
D���������¶ȣ�X���������������÷�Ӧ�ġ�H��0
�ο��𰸣�A
���������
�����Ѷȣ�һ��
3��ѡ���� һ���¶��¿��淴ӦN2(g) + 3H2(g)  ?2NH3(g) ��ƽ��ı�־��
?2NH3(g) ��ƽ��ı�־��
A��v��(N2) = v��(NH3)
B��v��(N2) = 3v��(H2)
C��v��(H2) =" 3/2" v��(NH3)
D��N2��H2��NH3�������Ϊ1�U3�U2
�ο��𰸣�C
�����������һ�������£������淴Ӧ������Ӧ���ʺ��淴Ӧ�������ʱ������Ϊ0�����������ʵ�Ũ�Ȼ��������ٷ����仯��״̬���ǻ�ѧƽ��״̬��ƽ��ʱŨ�Ȳ��ٷ����仯��������֮���Ũ�Ȳ�һ����Ȼ�����ij�ֹ�ϵ������C����ȷ��A��C�з�Ӧ���ʵķ����෴����A�в���������֮������Ӧ�Ļ�ѧ������֮�ȣ�����ȷ��C����������֮������Ӧ�Ļ�ѧ������֮�ȣ���ȷ��B�з�Ӧ���ʵķ�����ͬ�����Բ���˵������ѡC��
�����Ѷȣ�һ��
4��ѡ���� ij�¶��£���һ��2 L���ܱ������У�����4 mol A��2 mol B�������·�Ӧ��
3A(g)+2B(g) 4C(s)+2D(g)����Ӧһ��ʱ���ﵽƽ�⣬�������1.6 mol C��������˵����ȷ����?��?��
4C(s)+2D(g)����Ӧһ��ʱ���ﵽƽ�⣬�������1.6 mol C��������˵����ȷ����?��?��
A���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽ��K��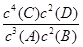
B����ʱB��ƽ��ת������40%
C���������ϵ��ѹǿ��ƽ�������ƶ�����ѧƽ�ⳣ������
D������B��ƽ�������ƶ���B��ƽ��ת��������
�ο��𰸣�B
�����������ѧƽ�ⳣ������һ�������£������淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�����Ը��ݷ�Ӧ�ķ���ʽ��֪A����ȷ����Ϊ������C�ǹ��壻����1.6molC��ͬʱ��Ȼ����0.8molB������B��ת������40%��B��ȷ��ƽ�ⳣ��ֻ���¶��й�ϵ���ı�ѹǿƽ�ⳣ�����䣬C����ȷ��ͬ��DҲ�Ǵ���ģ�ƽ�ⳣ�����䣬��ѡB��
�����������ǻ���������Ŀ��飬�ѶȲ�����ѧ�����״�ѡAѡ���Ҫ�����ڶԸ���IJ�������������ⲻ��ȷ���µġ���������������ѧ���Ĺ淶���⡢����������
�����Ѷȣ���
5��ѡ���� 440��ʱ2SO2(g) + O2(g) 2SO3(g) ��H����198kJ/mol���ڼס��ҡ��������ݻ���Ϊ2 L�ĺ����ܱ�������Ͷ��SO2(g)��O2(g)����5min�ﵽƽ�⡣����ʼ���ʵ�����SO2��ƽ��ת�������±���ʾ��
2SO3(g) ��H����198kJ/mol���ڼס��ҡ��������ݻ���Ϊ2 L�ĺ����ܱ�������Ͷ��SO2(g)��O2(g)����5min�ﵽƽ�⡣����ʼ���ʵ�����SO2��ƽ��ת�������±���ʾ��
| ? | �� | �� | �� | |
| ��ʼ���ʵ��� | n(SO2) / mol | 0.4 | 0.8 | 0.8 |
| n(O2) / mol | 0.24 | 0.24 | 0.48 | |
| SO2��ƽ��ת���� | 80% | ��1 | ��2 | |
�ο��𰸣�C
���������A��ƽ��ʱ����SO2�����ʵ�����0.4mol��0.8��0.32mol��Ũ����0.32mol��2L��0.16mol/L����˼���SO2������Ϊ0.16mol/L��5min��0.032mol��L-1��min-1��A����ȷ��B��ƽ��ʱSO2��Ũ����0.08mol/L��2L��0.04mol/L�����������Ũ����0.16mol/L��������Ũ���ǣ�0.24mol��0.16mol����2L��0.04mol/L�����Ը��¶��·�Ӧ��ƽ�ⳣ��K��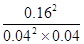 ?��400��B��ȷ��C������Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ�����淴Ӧ�����ƶ���ƽ�ⳣ����С��C����ȷ��D���������൱�����ڼ������Ļ�����������������Ũ�ȣ����������ת���ʽ��ͣ��������൱�����ڼ������Ļ���������ѹǿ��ƽ��������Ӧ�����ƶ������������ת��������D��ȷ����ѡC��
?��400��B��ȷ��C������Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ�����淴Ӧ�����ƶ���ƽ�ⳣ����С��C����ȷ��D���������൱�����ڼ������Ļ�����������������Ũ�ȣ����������ת���ʽ��ͣ��������൱�����ڼ������Ļ���������ѹǿ��ƽ��������Ӧ�����ƶ������������ת��������D��ȷ����ѡC��
�����Ѷȣ�һ��