时间:2020-08-13 06:54:52
1、选择题 用NA表示阿伏加德罗常数的值,下列说法中正确的是
A.28g氮气所含有的原子数目为NA
B.16g O2中所含的氧原子数为NA
C.标准状况下,22.4L水中含有NA个水分子
D.标准状况下,22.4L氯化氢所含的原子数为NA
参考答案:B
本题解析:略
本题难度:一般
2、选择题 在一个密闭容器中盛有11gCO2时,压强为1x104Pa.如果在相同温度下,把更多的CO2充入容器,使压强增至5x104Pa,这时容器内气体的分子数约为(?)
A.3.3x1025
B.3.3x1024
C.7.5x1023
D.7.5x1022
参考答案:C
本题解析:在相同的温度和体积下,气体的压强之比是气体的物质的量之比。11gCO2的物质的量是11g÷44g/mol=0.25mol,所以后来的CO2的物质的量是0.25mol×5x104Pa/1x104Pa=1.25mol,因此含有的分子数是1.25mol×6.02x1023 /mol=7.5x1023 ,答案选C。
本题难度:一般
3、填空题 2010年春,发生在滇、黔、桂、渝、川等省的严重旱情牵动了全国人民的心。水是组成生命体的重要化学物质,有关水的反应有很多。
(1)水分子自身作用会生成阴、阳两种离子,其中阳离子的电子式是 。
(2)在由水电离产生的c(H+)=1×10-14 mol·L-1的溶液中,①NH4+、Al3+、Br-、SO42- ② Na+、Mg2+、Cl-、NO3-③K+、Ba2+、Cl-、NO3- ④K+、Na+、HCO3-、SO42-四组离子中,一定可以大量共存的是 (填序号,下同),可能大量共存的是 。
(3)在下列反应中,水仅做氧化剂的是 (填字母,下同),水既不做氧化剂又不做还原剂的是 。
A.Cl2+H2O=HCl+HClO
B.2Na2O2+2H2O=4NaOH+O2↑
C.CaH2+2H2O=Ca(OH)2+2H2↑
D.3Fe+4H2O Fe3O4+4H2
Fe3O4+4H2
(4)“神舟七号”飞船上的能量主要来自于太阳能和燃料电池,H2、O2和KOH的水溶液可形成氢氧燃料电池,负极的电极反应为 ,电极反应产生的水经冷凝后可作为航天员的饮用水,当得到1.8 L饮用水时,电池内转移的电子数约为 。
(5)右图是某品牌饮用矿泉水标签的部分内容。请认真阅读标签内容后计算。
①该矿泉水中镁离子的物质的量浓度的最大值是 ;
②一瓶合格的这种矿泉水中硫酸根离子的物质的量不能超过 mol。
参考答案:(1)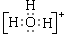
(2)③;①②
(3)CD;AB
(4)2H2+4OH--4e-=4H2O
(5)①2×10-4mol·L -1 ②1×10-4mol(每空2分)
本题解析:化学高考试题常常和时事联系很紧密。
(1)水分子自身作用的方程式为2H2O H3O++OH-;
H3O++OH-;
(2)“由水电离产生的c(H+)=1×10-14 mol·L-1的溶液”即溶液的pH可能为14也可能为0;即“可以为酸性溶液,也可能为碱性溶液”。①中NH4+、Al3+在碱性溶液中不能存在,②中Mg2+在碱性溶液中不能存在,④中HCO3-在酸性溶液或者碱性溶液中均不能存在;
(3)水中氢元素化合价只有降低的反应水仅做氧化剂,水中氢元素化合价不变的反应水既不做氧化剂也不做还原剂;
(4)原电池的负极反应为氧化反应,结合总反应2H2+O2=2H2O,可得负极反应;1.8 L水的质量为1800g,即100mol,生成100mol水转移电子200mol,即1.204×1026或者200NA;
(5)c(Mg2+)≤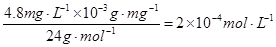
n(SO42-)≤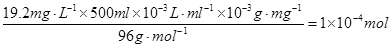 。
。
本题难度:困难
4、选择题 0.5L?1mol/L?FeCl3溶液与0.2L?1mol/L?KCl溶液中的Cl-的物质的量浓度之比( )
A.5:2
B.3:1
C.15:2
D.1:3
参考答案:0.5L?1mol/L?FeCl3溶液中c(Cl-)=3c(FeCl3)=3×1mol/L=3mol/L;
0.2L?1mol/L?KCl溶液中c(Cl-)=c(KCl)=1mol/L,
所以0.5L?1mol/L?FeCl3溶液与0.2L?1mol/L?KCl溶液中的Cl-的物质的量浓度之比为3mol/L:1mol/L=3:1,
故选B.
本题解析:
本题难度:一般
5、选择题 在1 L 1 mol.L-1纯碱溶液中逐滴加入200mL 3.5 mol/L的硫酸,完全反应后生成标准状况下的CO2是? (? )
A.0L
B.8.96L
C.15.68 L
D.26.88L
参考答案:B
本题解析:碳酸钠的物质的量是1mol,稀硫酸的物质的量是0.2L×3.5mol/L=0.7mol。碳酸钠和稀硫酸反应的方程式是
CO32-+H+=HCO3-
1mol? 1mol 1mol
HCO3-+H+=H2O+CO2↑
0.4mol 0.4mol? 0.4mol
所以在反应中生成的CO2的物质的量是
在标准状况下的体积是0.4mol×22.4L/mol=8.96L,答案选B。
点评:该题答题时明确“碳酸钠先和酸反应生成碳酸氢钠,然后碳酸氢钠再和酸反应生成二氧化碳”的过程是解本题的关键,属于中等难度的试题,有利于培养学生的逻辑推理能力和发散思维能力。
本题难度:一般