时间:2020-08-13 06:46:57
1、选择题 1820年德贝莱纳用MnO2作催化剂使KClO3分解产生O2,发现制得的O2有异常气味,使该气体通过淀粉碘化钾溶液,溶液变蓝色,则氧气中可能混有(? )
①Cl2?②Br2?③NO2?④O3?⑤CO2
A.①②
B.②③
C.①④
D.全部
参考答案:C
本题解析:由于制得的气体能使淀粉碘化钾溶液变蓝,说明具有较强氧化性的气体生成,且由MnO2、KClO3的组成根据元素守恒排除Br2、NO2、CO2,可能为Cl2、O3。
本题难度:简单
2、选择题 在一集气瓶充入1/2体积H2,1/4体积N2,1/4体积Cl2,光照使之爆炸后,倒置于水槽中,最后进入集气瓶中的水的体积应该是:
A.1/3体积
B.1/4体积
C.1/2体积
D.2/3体积
参考答案:C
本题解析:略
本题难度:一般
3、选择题 用氯气跟单质化合不能制取的物质是
A.KCl
B.FeCl2
C.FeCl3
D.CuCl2
参考答案:B
本题解析:铁在氯气中燃烧生成的氯化铁,得不到氯化亚铁,选项B不正确,其余选项都是正确的,答案选B。
点评:该题是基础性试题的考查,难度不大。该题的关键是熟练记住金属单质和氯气的反应产物,属于识记性知识的检验。
本题难度:一般
4、填空题 (4分)(1)写出电解饱和食盐水的 离子方程式____________________________________________
离子方程式____________________________________________
(2)写出工业上用氯气和石灰乳为原料制造漂白粉的化学方程式______________________
参考答案: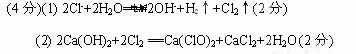
本题解析:略
本题难度:简单
5、填空题 某含氯化合物A由两种短周期元素组成,常温下该物质为气态,测得该气体对空气的相对密度为3.0,A溶于水可得只含单一溶质B的弱酸性溶液,B溶液在放置过程中其酸性会增强。常温下,气体A与NH3反应生成离子晶体C、气体单质D和常见液体E,D为空气中含量最多的物质。气体A可用某一气体单质与潮湿的Na2CO3反应制得,同时生成两种钠盐。请回答下列问题:
(1)气体A的化学式为?,气体单质D对应元素在周期表中的位置为?。
(2)用化学方程式表示B溶液酸性增强的原因?。
(3)气体A与NH3反应的化学方程式为?,该反应体现气体A具有?性。
(4)试写出制取气体A的化学方程式为??。
(5)设计实验探究离子晶体C的成分为?。
参考答案:(1)Cl2O;第二周期第ⅤA族
(2)2HClO=2HCl+O2
(3)3Cl2O+10NH3=6NH4Cl+2N2+3H2O;?氧化
(4)2Cl2+2Na2CO3+H2O=Cl2O+2NaHCO3+2NaCl
(5)取少量晶体溶于水,分成两份于试管中;一份加入浓NaOH溶液、加热,若产生能使湿润的红色石蕊试纸变蓝的气体,证明含有NH4+;另一份加入用硝酸酸化的硝酸银溶液,产生白色沉淀,证明含Cl-,由此证明该晶体为NH4Cl。A与氨气生成离子晶体C,C是NH4Cl,由于氯元素的化合价发生变化,氨气中的氮化合价必然升高,其氧化产物是N2,这利用了A的氧化性
本题解析:本题是元素及化合物综合运用题。A的相对分子质量为29×3=87,而Cl的相对原子质量为35.5,所以Cl原少至少为2个,这样O为1个,A合理的分子式为Cl2O;根据化合价规律,A溶于水生成弱酸B为HClO;值得注意的是A和氨反应方程式的书写,是近几年高考考查能力最多的一种体验,要用心学会如何书写。另外最后一问是“离子晶体”证明设计,要设法证明既有NH4+又有Cl-离子存在,这才是完全理解题意,设计步骤要完整规范。
本题难度:一般