时间:2020-08-13 06:41:27
1、填空题 磷在自然界常以难溶于水的磷酸盐如Ca3(PO4)2等形式存在。它的单质和化合物有着广泛的应用。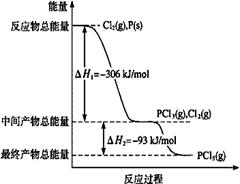
(1)红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。
请回答问题:
①PCl5分解成PCl3和Cl2的热化学方程式是 。
②P和Cl2分两步反应生成1 mol PCl5的△H3= 。
(2)PCl5分解成PCl3和Cl2的反应是可逆反应。T℃时,向2.0 L恒容密闭容器中充入1.0 mol PCl5,经过250 s达到平衡。反应过程中测定的部分数据见下表:
| t / s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3) / mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
参考答案:(1)①PCl5(g)=PCl3(g)+Cl2(g)△H=+93kJ/mol(2分,方程式1分,△H的表示1分,化学式、状态错误0分;+、焓变数值、单位错漏合扣1分;计量数用分数表示与焓变相匹配也给分)
②-399 kJ/mol(2分,单位错漏扣1分)
(2)①1.5×10-4mol/(L・s) 或0.00015 mol/(L・s)(2分,单位错漏扣1分)
②2.5×10-2 mol/L或0.025mol/L
(3)①9~10.5(2分,介于此区间或区间内的某一点)
c(H2PO4-)>c(HPO42-) (2分)
②Na2HPO4溶液中存在电离平衡,HPO42- H++PO43-(1分),加入CaCl2溶液,Ca2+与PO43-结合生成Ca3(PO4)2沉淀,促使Na2HPO4电离平衡向右移动,H+浓度增大,溶液显酸性(1分)。(合理即给分)
H++PO43-(1分),加入CaCl2溶液,Ca2+与PO43-结合生成Ca3(PO4)2沉淀,促使Na2HPO4电离平衡向右移动,H+浓度增大,溶液显酸性(1分)。(合理即给分)
本题解析:(1)①题干中特别注明图中物质转化的焓变是生成1mol产物的数据,因此PCl5分解成PCl3和Cl2是吸热反应,其热化学方程式为:PCl5(g)=PCl3(g)+Cl2(g)△H=+93kJ/mol;
②计算P和Cl2分两步反应生成1 mol PCl5 的焓变,根据盖斯定律反应的焓变与过程无关,只需将图像中两部分的焓变相加即可,所以△H3=-399 kJ/mol。
(2)①计算反应在50~150s 内的用PCl3表示的反应速率,只需把数据代入公式,因此有v(PCl3)=△C/△t=(0.19-0.16)mol/(2L×100s)= 1.5×10-4mol/(L・s);
② PCl5(g) = PCl3(g)+Cl2(g)
起始浓度(mol/L)  =0.50 0 0
=0.50 0 0
转化浓度(mol/L) 0.10  =0.10 0.10
=0.10 0.10
平衡浓度(mol/L) 0.40 0.10 0.10 (1分)
K= 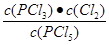 =
=  = 2.5×10-2 mol/L或0.025mol/L
= 2.5×10-2 mol/L或0.025mol/L
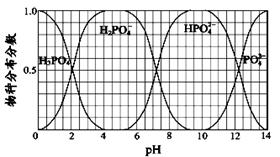
(3)此题要学会认真读图,该图表示的是H3PO4与不断加入的NaOH反应,氢氧化钠量不断增大使溶液pH值不断增大时,溶液中各含磷物种的百分比。每个含磷物种在一定的PH范围内都有百分含量极大和极小的情况,而两条线交叉部分表示的则是2种含磷物种同时存在的情况。
①要获得叫纯净的Na2HPO4,则通过图像找到PH值在9~10.5的范围内,HPO42- 的百分含量接近百分百,所以控制的PH只要在这个范围内,都可以获得较纯净的Na2HPO4 。
②Na2HPO4是弱酸酸式盐,HPO42-存在电离和水解两个平衡,由于溶液呈碱性,可以看出水解强于电离。但是该盐溶液加入氯化钙后,溶液呈酸性,因此可以推测加入的氯化钙一定改变了电离平衡,使之不断产生出氢离子,使溶液呈酸性。所以结合本题的题干“磷在自然界常以难溶于水的磷酸盐如Ca3(PO4)2等形式存在”,可以解释平衡的移动为:Na2HPO4溶液中存在电离平衡,HPO42- H++PO43-,加入CaCl2溶液,Ca2+与PO43-结合生成Ca3(PO4)2沉淀,促使Na2HPO4电离平衡向右移动,H+浓度增大,溶液显酸性。
H++PO43-,加入CaCl2溶液,Ca2+与PO43-结合生成Ca3(PO4)2沉淀,促使Na2HPO4电离平衡向右移动,H+浓度增大,溶液显酸性。
考点:本题考查的是反应原理的知识,侧重于化学与反应能量的关系、反应速率和平衡常数计算、平衡移动原理解释等方面的考查。
本题难度:困难
2、填空题 (1)三种弱酸HA、H2B、HC,电离常数的数值为1.8×10-5、5.6×10-11、4.9×10-10、4.3×10-7(数据顺序已打乱),已知三种酸和它们的盐之间能发生以下反应:
①HA+HB-(少量)=A-+H2B
②H2B(少量)+C-=HB-+HC
③HA(少量)+C-=A-+HC
则三种酸对应的电离常数分别为(请填空)
| HA | H2B | HC Ka Ka1 Ka2 Ka 数值 1.8×10-5 4.3×10-7 ______ ______ | ||
参考答案:(1)根据溶液中强酸制弱酸的原理以及反应H2B(少量)+C-=HB-+HC,可以确定酸性强弱是:H2B>HC>HB-,
故答案为:5.6×10-11;4.9×10-10;
(2)①根据溶液中的电荷守恒:c(Na+)+c(H+)=c(HD-)+2c(D2-)+c(OH-),当溶液的pH=7时,c(H+)=c(OH-),所以c(Na+)=c(HD-)+2c(D2-),故答案为:c(HD-)+2c(D2-);
?②0.1mol?L-1的H2D水溶液中,用氢氧化钠来调节溶液pH,得到含有H2D、HD-、D2-三种微粒的溶液,说明溶液依旧呈酸性,H2D为二元酸,当加入氢氧化钠不足量时,会发生反应:NaOH+H2D=NaHD+H2O,根据物料守恒则有c(Na+)=c(D2-)+c(HD-)+c(H2D),故答案为:NaHD.
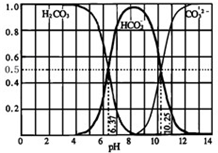
(3)①A、由图可知,pH=2时溶液中含H2CO3,而没有HCO3-、CO32-,故A错误;
B、由图可知,pH为6.37时c(H2CO3)=c(HCO3-),pH为10.25时,c(HCO3-)=c(CO32-),但三者的浓度不相等,故B错误;
C、由图可知,pH为7.4时,HCO3-的最大,则当人体血液的pH约为7.4,则CO2在血液中多以HCO3-的形式存在,故C正确;
D、由图可知,pH大于12时,溶液中主要存在CO32-,则用CO2和NaOH反应制取Na2CO3,溶液的pH必须控制在12以上,故D正确;
故选CD;
②在10mL1mol/LNa2CO3溶液中加入某浓度的盐酸后,当调节溶液的pH=10.25时,据图中内容可以看出:HCO3-、CO32-两种成分平衡时的组成分数分别为50%,即碳酸钠和碳酸氢钠的物质的量分别是0.005mol,此时溶液的体积恰好为100mL,所碳酸钠中碳酸根的浓度是0.05mol/L,再加入1mL1×10-4mol?L-1的CaCl2稀溶液时,Qc=c(Ba2+)?c(CO32-)=0.05mol/L×10-6mol/L=5×10-8(mol/L)2,而Ksp(CaCO3)=5.0×10-9,所以Qc>Ksp,能生成沉淀,故答案为:是.
本题解析:
本题难度:一般
3、选择题 下列关于电解质溶液的叙述正确的是( )
A.常温下,pH=7的NH4Cl与氨水的混合溶液中离子浓度大小顺序:c(Cl-)>c(NH4+)>c(H+)=c(OH-)
B.将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低
C.中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同
D.常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大
参考答案:A.常温下,pH=7的溶液中c(H+)=c(OH-),溶液中存在电荷守恒,所以c(Cl-)+c(OH-)=c(NH4+)+c(H+),所以c(Cl-)=c(NH4+),故A错误;
B.醋酸是弱电解质,稀释醋酸溶液时促进醋酸电离,醋酸根离子和氢离子浓度都减小,温度不变,水的离子积常数不变,所以氢氧根离子浓度增大,故B错误;
C.pH相等的醋酸和盐酸溶液,醋酸的物质的量浓度大于盐酸,等体积等PH的醋酸和盐酸溶液,消耗的氢氧化钠的物质的量与酸的物质的量成正比,所以醋酸消耗的氢氧化钠溶液多,故C错误;
D.常温下,硫离子的第一步水解程度大于第二步,所以同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大,故D正确;
故选D.
本题解析:
本题难度:简单
4、选择题 对室温下体积相同,浓度均为0.1mol?L-1的盐酸和醋酸两种溶液分别采取下列措施.有关叙述中一定正确的是( )
A.加人足量的小苏打固体充分反应后,两溶液中产生的CO2一样多
B.加入NaOH固体恰好中和后,两溶液的pH相同
C.分别加入足量锌粉充分反应,反应开始时两酸产生H2的反应速率相等
D.加水稀释100倍后,两溶液的pH相同
参考答案:A、体积相同,浓度均为0.1mol?L-1的盐酸和醋酸两种溶液溶质物质的量相同,都是一元酸和碳酸氢钠反应生成二氧化碳相同,故A正确;
B、加入NaOH固体恰好中和后盐酸溶液pH=7,醋酸钠会发生水解反应,pH>7,故B错误;
C、体积相同,浓度均为0.1mol?L-1的盐酸和醋酸两种溶液中,醋酸是弱电解质存在电离平衡,溶液中的氢离子浓度小于盐酸中的氢离子浓度,所以加入锌时,盐酸的反应速率要快于醋酸,故C错误;
D、加水稀释100倍后,盐酸溶液的pH增大2各单位,醋酸是弱酸,氢离子浓度小,PH大于盐酸,故D错误;
故选A.
本题解析:
本题难度:一般
5、选择题 H2SO3、H2CO3分别属于中强酸和弱酸,H2SO3 ?H+ + HSO3-? HSO3-
?H+ + HSO3-? HSO3- ?H+ + SO32-? H2CO3
?H+ + SO32-? H2CO3 ?H+ + HCO3-;HCO3-
?H+ + HCO3-;HCO3- ?H+ + CO32-;已知K1 > K1" ≈ K2 > K2",则溶液中不可以大量共存的离子组合是(?)
?H+ + CO32-;已知K1 > K1" ≈ K2 > K2",则溶液中不可以大量共存的离子组合是(?)
A.SO32-、HCO3-
B.HSO3-、CO32-
C. SO32-、CO32-
D.HSO3-、HCO3-
参考答案:B
本题解析:略
本题难度:简单