时间:2020-08-13 06:20:07
1、简答题 A、B、C、D、E分别属于周期表中前20号元素,其原子序数依次递增,并且其中只有一种金属元素.A是元素周期表所有元素中原子半径最小的;B和C?都只有两个电子层,B中一层电子数是另一层的两倍;C?中两层电子数之和是两层电子数之差的两倍;?D中一层电子数是另两层电子数之和;E?核外各层电子数两两相等.
请按要求回答下列问题:
(1)画出E?的离子结构示意图______,写出由A?和C?组成的含有非极性键的化合物的电子式______.
(2)由上述元素组成的化合物中属于极性键构成的非极性分子是______.?(只要求写出两种,用化学式表示)
(3)由C?与E?形成的化合物高温时与B反应生成两种化合物,请写出该反应的化学方程式______
(4)写出上述元素形成的化合物中一种可溶性的正盐与另一种强酸反应的离子方程式:______
(5)上述元素形成的化合物中通常能污染空气的是______?(至少写出两种).某一种可污染空气的化合物与强氧化剂单质常温下反应生成两种化合物,该反应的化学方程式为:______.
参考答案:A是元素周期表所有元素中原子半径最小的,则A为H元素;E核外各层电子数两两相等,则E为Ca元素.
A、B、C、D、E分别属于周期表中前20号元素,其原子序数依次递增,并且其中只有一种金属元素.B中一层电子数是另一层的两倍,则B为C元素;C?中两层电子数之和是两层电子数之差的两倍,则C为O元素;D中一层电子数是另两层电子数之和,则D为S元素.
即A为H元素;B为C元素;C为O元素;D为S元素;E为Ca元素.
(1)E为Ca元素,Ca2+核内质子数为20,核外18个电子,有3个电子层,最外层有8个电子,离子结构示意图为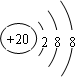
.
A和C组成的含有非极性键的化合物是H2O2,过氧化氢电子式为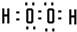
.
故答案为:
;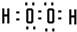
.
(2)上述元素组成的化合物中属于极性键构成的非极性分子有CH4、CO2、CS2.
故答案为:CH4、CO2、CS2.
(3)由C与E形成的化合物为CaO,高温时与碳反应生成CaC2和CO,反应方程式为CaO+3C?高温?.?CaC2+CO↑.?
故答案为:CaO+3C?高温?.?CaC2+CO↑.
(4)上述元素组成的可溶性盐为醋酸钙,强酸为硫酸,反应离子方程式为Ca2++2CH3COO-+2H++SO42-=2CH3COOH+CaSO4↓.
故答案为:Ca2++2CH3COO-+2H++SO42-=2CH3COOH+CaSO4↓.
(5)上述元素形成的化合物中通常能污染空气的是CO、SO2、H2S?等;
臭氧具有强氧化性,硫化氢具有较强的还原性,二者发生反应?H2S+O3=SO2+H2O.
故答案为:CO、SO2、H2S?等;H2S+O3=SO2+H2O.
本题解析:
本题难度:一般
2、选择题 R为1~18号元素,其原子所具有的电子层数为最外层电子数的
| 1 2 |
参考答案:R为1~18号元素,其原子所具有的电子层数为最外层电子数的12,若R的电子层为1,则核外电子数为2,为He元素,He性质稳定,没有含氧酸根;若R的电子层为2,则最外层电子数为4,为C元素;若R的电子层为3,则最外层电子数为6,为S元素.
A、当R可以形成①R2 O42-时,是C2 O42-,故R为C元素,C元素可以形成CO32-,故A错误;
B、当R可以形成②RO42-时,R为+6价,故R为S元素,S元素可以形成S2 O32-,SO32-,故B正确;
C、当R可以形成①R2 O42-时,是C2 O42-,故R为C元素,C元素不可能形成RO42-、R2O32-形式结构的离子,故C正确;
D、当R可以形成②RO42-时,R为+6价,故R为S元素,S元素可以形成S2 O32-,SO32-,不可能形成R2 O42-形式结构的离子,故D错误.
故选:BC.
本题解析:
本题难度:简单
3、选择题 有a、b、c、d四种主族元素,已知a、b的阳离子和c、d的阴离子都具有相同的电子层结构,而且原子半径a>b,阴离子所带负电荷数c>d,则四种元素的原子序数关系是( )
A.a>b>c>d
B.b>a>d>c
C.c>b>a>d
D.b>a>c>d
参考答案:a、b元素的阳离子和c、d元素的阴离子都具有相同的电子层结构,则a、b元素的原子序数大于c、d元素的原子序数,
同周期元素从左到右原子半径逐渐减小,原子半径a>b,则a的原子序数小于b,
同周期元素从左到右原子的最外层电子数逐渐增多,c的阴离子所带负电荷比d的阴离子所带负电荷多,则d的最外层电子数比c多,所以d的原子序数大于c,
所以四种元素的原子序数大小关系为b>a>d>c,
故选B.
本题解析:
本题难度:简单
4、填空题 短周期主族元素A、B、C、D的原子序数依次增大,A与D同主族,B与C在同一周期,B原子最外层电子数比C原子少2个,A、C单质在常温下均为气体,它们在一定条件下以体积比2:1完全反应,生成物在常温下是液体.此液体与D单质在常温下能剧烈反应生成A的单质.所得溶液滴入酚酞显红色.回答下列问题:
(1)写出元素符号A______,B______,C______,D______.
(2)写出B与C两种单质完全反应后所得生成物的电子式______,该分子空间构型为______.
(3)C、D两种单质在点燃条件下形成的化合物的电子式 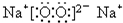
,判断其中的化学键的类型______.
(4)写出两种由A、B、C、D四种元素组成的化合物的化学式______、______.
参考答案:根据A、C单质在常温下均为气体,它们在一定条件下以体积比2:1完全反应,生成物在常温下是液体.可知液体是水,A为氢气,C为氧气;根据水与D单质在常温下能剧烈反应生成A的单质,所得溶液滴入酚酞显红色,且A与D同主族,短周期主族元素,可知D为钠;根据B与C在同一周期,B原子最外层电子数比C原子少2个,可知B为碳,
(1)因A为氢气,B为碳,C为氧气,D为钠,四种元素的元素符号分别是:H、C、O、Na、故答案为:H;C;O;Na.
(2)因碳与氧气完全反应后生成二氧化碳,故答案为: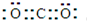
; 直线形;
(3)因过氧化钠中既有钠离子和过氧根离子之间的离子键又有氧原子和氧原子之间的共价键,故答案为:离子键,非极性键;
(4)Na、H、C、O四中元素四种元素组成的化合物有NaHCO3、CH3COONa,故答案为:NaHCO3;CH3COONa.
本题解析:
本题难度:一般
5、选择题 元素性质存在周期性变化的本质原因是( )
A.元素原子相对原子质量周期性变化的结果
B.元素原子核外电子排布周期性变化的结果
C.元素的原子序数递增的结果
D.元素金属性和非金属性周期性变化的结果
参考答案:B
本题解析:
本题难度:一般