时间:2020-08-13 06:14:18
1、选择题 为了降低某水库的铁闸门被腐蚀的速率,焊接在铁闸门上的固体材料可以采用
[? ]
A.铜
B.钠
C.锌
D.石墨
参考答案:C
本题解析:
本题难度:简单
2、选择题 下列叙述正确的是?
[? ]
A.在原电池的负极和电解池的阴极上都发生失电子的氧化反应
B.用惰性电极电解Na2SO4溶液,阴、阳两极产物的物质的量之比为1∶2
C.用惰性电极电解饱和NaCl溶?液,若有1?mol电子转移,则生成1?mol?NaOH
D.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀
参考答案:C
本题解析:
本题难度:一般
3、选择题 近年来,加“碘”食盐较多的使用了碘酸钾(KIO3),碘酸钾在工业上可用电解法制取。以石墨和不锈钢为电极,以KI溶液为电解液,在一定条件下电解,反应的化学方程式为:KI+3H2O KIO3+3H2↑。下列有关说法不正确的是
KIO3+3H2↑。下列有关说法不正确的是
A.电解时,石墨作阳极,不锈钢作阴极
B.电解时的阳极电极反应式:I-?6e-+3H2O = IO3-+6H+
C.当电解过程中转移3 mol e-时,理论上可制得KIO3 107 g
D.电解一段时间后,电解质溶液的pH变小
参考答案:D
本题解析:
A、电解时I-失电子生成IO3-,不锈钢不能作阳极,正确;
B、阳极I-失电子生成IO3-,根据电子、电荷守恒、质量守恒配平,正确;
C、反应KI+3H2O KIO3+3H2↑每生成1mol KIO3转移6mol电子,正确;
KIO3+3H2↑每生成1mol KIO3转移6mol电子,正确;
D、电解一段时间,pH不变,错误。
本题难度:一般
4、选择题 观察下列几个装置示意图,有关叙述正确的是 ( ? )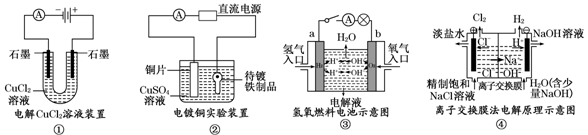
A.装置①中阳极上析出红色固体
B.装置②的待镀铁制品应与电源正极相连
C.装置③中外电路电子由a极流向b极
D.装置④的离子交换膜允许阳离子、阴离子、水分子自由通过
参考答案:C
本题解析:A 阳极: 2Cl--2e-=Cl2?阴极:Cu2++2e-=Cu?装置①中阴极上析出红色固体,A错误。
B?阳极:Cu-2e-=Cu2+?阴极:Cu2++2e-=Cu?待镀金属制品做阴极,镀层金属做阳极,含有镀层金属离子的溶液做电镀液,装置②的待镀铁制品应与电源负极相连,B错误。氢氧燃料电池中氢气人口为负极,氧气人口为正极,电子有负极流到正极,由a极流向b极,C正确。装置④的阳离子交换膜允许阳离子通过,不允许阴离子及气体通过;石棉隔膜阻止气体通过,但允许水分子及离子通过,D错误。
本题难度:简单
5、选择题 右图是模拟铁的电化学防护装置。以下叙述正确的是(?)
A.此装置属于电解池
B.此装置中的铁极上发生氧化反应
C.该电化学防护法称为“牺牲阳极阴极保护法”
D.该电化学防护法称为“外加电源阴极保护法”
参考答案:C
本题解析:
正确答案C
A.不正确,没有外加电源,此装置属于原电池
B.不正确,此装置中的铁极上发生还原反应:O2+4e―+2H2O=4OH―
C.正确
D.不正确。该电化学防护法称为“牺牲阳极阴极保护法”
本题难度:一般