时间:2020-08-13 05:35:39
1、实验题 下列方法中,能用于实验室制取氨的是??
①在烧瓶中将熟石灰和氯化铵混合,加水调成泥状后加热
②加热试管中的氯化铵固体
③将烧瓶中的浓氨水加热
④将分液漏斗中的浓氨水滴入装有生石灰的烧瓶中
参考答案:①③④
本题解析:①Ca(OH)2+2NH4Cl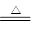 CaCl2+2NH3↑+H2O,正确
CaCl2+2NH3↑+H2O,正确
②虽然NH4Cl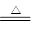 NH3↑+HCl↑有氨气逸出,但NH3+HCl=NH4Cl,不正确
NH3↑+HCl↑有氨气逸出,但NH3+HCl=NH4Cl,不正确
③NH3・H2O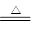 NH3↑+H2O,正确
NH3↑+H2O,正确
④CaO+H2O=Ca(OH)2有大量OH-生成,使平衡NH4++OH- NH3・H2O
NH3・H2O NH3+H2O右移,有得氨气的生成;另外放出大量的热,使反应NH3・H2O
NH3+H2O右移,有得氨气的生成;另外放出大量的热,使反应NH3・H2O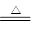 NH3↑+H2O有氨气逸出,正确
NH3↑+H2O有氨气逸出,正确
故答案为①③④
本题难度:简单
2、选择题 下列反应属于氮的固定的是(?)
A.空气在雷电作用下所产生NO
B.NO和O2生成NO2
C.铜与浓硝酸反应产生NO2
D.NH4Cl与Ca(OH)2反应生成NH3
参考答案:A
本题解析:略
本题难度:简单
3、填空题 【化学―选修2:化学与技术】(15分)
I、污水经过一级、二级处理后,还含有少量Cu2+、Hg2+、Pb2+等重金属离子,可加入沉淀剂使其沉淀。下列物质不能作为沉淀剂的是
A.氨水
B.硫化氢气体
C.硫酸钠溶液
D.纯碱溶液
II、合成氨的流程示意图如下: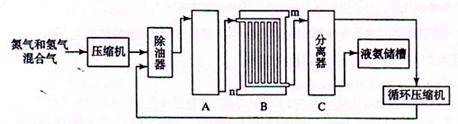
回答下列问题:
(1)工业合成氨的原料是氮气和氢气。氮气是从空气中分离出来的,通常使用的两种分离方法是?,?;氢气的来源是水和碳氢化合物,写出分别采用煤和天然气为原料制取氢气的化学反应方程式?,
?;
(2) 设备A中含有电加热器、触煤和热交换器,设备A的名称?,其中发生的化学反应方程式为?;
(3) 设备B的名称?,其中m和n是两个通水口,入水口是?(填“m”或“n”)。不宜从相反方向通水的原因?;
(4) 设备C的作用?;
(5)在原料气制备过程中混有CO对催化剂有毒害作用,欲除去原料气中的CO,可通过如下反应来实现:CO(g)+H2O(g) ?CO2 (g)+ H2 (g) ,?已知1000K时该反应的平衡常数K=0.627,若要使CO的转化超过90%,则起始物中c(H2O):c(CO)不低于?。
?CO2 (g)+ H2 (g) ,?已知1000K时该反应的平衡常数K=0.627,若要使CO的转化超过90%,则起始物中c(H2O):c(CO)不低于?。
参考答案:Ⅰ、AC (2分)
Ⅱ、(1) 液化、分馏 ; (1分)?与碳反应除去CO2?(1分) (1分)?
(1分)? ?(1分)
?(1分)
(2) 合成塔? (1分) (1分)
(1分)
(3)冷却塔?(1分)? n (1分)
高温气体由冷却塔的上端进入,冷却水从下端进入,逆向冷却效果好。(2分)
(4)将液氨与未反应的原料气分离。 (1分)
(5)13.8? (2分)
本题解析:I.过量氨水与Cu2+反应生成[Cu(NH3)2]2+、硫酸钠溶液与Cu2+不反应。
Ⅱ⑴从空气中分离出氮气的方法:①先通过降温将空气液化,然后再升温分馏得氮气,②将空气与碳反应,然后再除去CO2得氮气;C、CH4均能与水蒸气反应制取氢气。
⑵工业上合成氨( )的设备为合成塔;
)的设备为合成塔;
⑶从合成塔出来的混合气(N2、H2、NH3)通过冷却塔使氨气冷凝从混合气中分离出来;冷却水要从下口(n)进入,高温气体由冷却塔的上端进入,实现逆向冷却效果好。
⑷设备C能将液氨与未反应的原料气分离出来,同时再将未反应的原料气压缩到合成塔中循环利用。
⑸据题意,要使反应正向进行(除去CO),则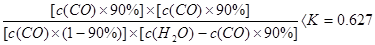 ,解得
,解得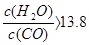 。
。
本题难度:一般
4、选择题 白磷(P4)分子呈正四面体结构(如右图所示),科学家受白磷分子的启发,又合成了结构和白磷分子类似的N4分子,下列关于P4和N4分子的说法正确的是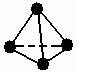
A.P4和N4是同系物
B.P4和N4?是同素异形体
C.P4和N4分子中各原子最外电子层均未达到8电子稳定结构
D.白磷比红磷活泼,N4比N2活泼
参考答案:D
本题解析:略
本题难度:一般
5、选择题 将35.8 g Al、Fe、Cu组成的合金溶于足量的NaOH溶液中,产生6.72 L气体(标准状况)。另取等质量的该合金溶于过量的稀硝酸中,生成13.44 LNO(标准状况),向反应后的溶液中加入足量的NaOH溶液,得到沉淀的质量为?(?)
A.50.8 g
B.66.4 g
C.44.8g
D.39.2g
参考答案:A
本题解析:在氢氧化钠溶液中发生反应:2Al+2NaOH+2H2O=2NaAlO2+3H2↑.n(H2)=6.72L÷22.4L/mol=0.3mol.所以n(Al)=0.2mol.m(Al)=5.4g,原混合物中铁、铜的质量和是30.4g在硝酸中发生反应:Al+4HNO3=Al(NO3)3+NO↑+2H2O;Fe++4HNO3=Fe(NO3)3+NO↑+2H2O;3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O.向反应后的溶液中加入足量的NaOH溶液,得到沉淀是氢氧化铝和氢氧化铜沉淀。铝与硝酸反应放出NO气体的物质的量为0.2mol.n(NO)总=13.44L÷22.4L/mol=0.6mol.所以;铁、铜与硝酸反应放出NO气体是0.4mol.可根据铁、铜的质量和是30.4g及;铁、铜与硝酸反应放出NO气体是0.4mol计算出铁、铜的质量,进而得到产生的沉淀的质量。选项为:A。
本题难度:一般