时间:2020-08-13 05:34:37
1、填空题 用镁铝合金的废料头、稀硫酸、氢氧化钠溶液制取MgCl2溶液和Al2(SO3)3溶液,只需通过四步反应完成,请依次写出其化学方程式:
(1)____________________________________。
(2)_______________________?_________。
(3)____________________________________。
(4)___________________________?_____。
参考答案:(1)2Al+2NaOH+2H2O=2NaAlO2+3H2↑
(2)2NaAlO2+H2SO4+2H2O=Na2SO4+2Al(OH)3↓
(3)2Al(OH)3+3H2SO4=Al2(SO4)3+6H2O
(4)Mg+2HCl=MgCl2+H2↑
本题解析:首先要利用镁和铝的性质不同,将镁和铝分离开,然后再按照要求通过一定化学反应制备目标产物。所利用的反应规律在初中化学里同学们已经学过了,此处实际也是一个复习过程。
本题难度:简单
2、选择题 1989年,世界卫生组织把铝确定为食品污染源,下列铝的应用应该加以控制的是( )
A.制铝合金
B.制电线
C.制防锈油漆
D.制易拉罐
参考答案:A、制造铝合金主要应用在住和行方面,不会污染人们的食物,无需控制;
B、制造电线应用了铝的导电性,也不会污染食品,无需控制;
C、制防锈漆,正常情况下铝与人的消化系统不直接接触,无需控制;
D、铝制易拉罐中的铝可能随饮料进入人体,需控制.
故选D.
本题解析:
本题难度:一般
3、选择题 将a mol钠和a mol铝一同投入m g足量水中,所得溶液密度为d g・mL-1,该溶液的溶质质量分数为(?)
A. %
%
B.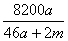 %
%
C.a/2%
D.3a/2%
参考答案:C
本题解析:由2Na+2H2O 2NaOH+H2↑,2Al+2NaOH+2H2O
2NaOH+H2↑,2Al+2NaOH+2H2O 2NaAlO2+3H2↑可知:
2NaAlO2+3H2↑可知:
2Na? ―? 2NOH? ―? H2↑
a mol? a mol? a/2?mol
2Al? ―? 2NaOH? ―? 2NaAlO2?―? 3H2↑
a mol? a mol?a mol?3a/2?mol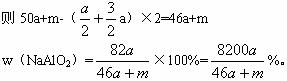
本题难度:简单
4、选择题 将由等物质量的铝、镁组成的混合物分成四等份,分别加入足量的①3mol/LNaOH溶液,②2mol/L稀硝酸(还原产物仅有NO),③18mol/LH2SO4,④1mol/LH2SO4产生气体物质的量由小到大的顺序为(? )
A.①②③④
B.②③①④
C.④②①③
D.③①②④
参考答案:D
本题解析:设每一份中金属的物质的量都是1mol,则①中生成1.5mol氢气,②中生成5/3mol,③中生成1molSO2(铝被钝化,不产生气体),④中生成2.5mol氢气,所以产生气体物质的量由小到大的顺序为③①②④,答案选D。
本题难度:一般
5、选择题 下列关于Al(OH)3的性质叙述错误的是
[? ]
A.Al(OH)3是两性氢氧化物
B.Al(OH)3是难溶于水的白色胶状物质
C.Al(OH)3能凝聚水中的悬浮物,也能吸附色素
D.Al(OH)3既能溶于NaOH溶液、氨水,又能溶于盐酸
参考答案:D
本题解析:
本题难度:简单