时间:2020-08-13 05:25:02
1、选择题 设NA为阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,22.4LCCl4含有C-Cl键的数目为4NA
B.常温常压下,44 g由N2O与CO2组成的混合气体含有的氧原子数目为NA
C.反应NH4N3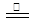 2N2↑+2H2↑,常温常压下每生成22.4LlN2,转移电子的数目为4NA
2N2↑+2H2↑,常温常压下每生成22.4LlN2,转移电子的数目为4NA
D.1 L 1 mol・L-1的AlCl3溶液中含有Cl-的数目为3NA
2、填空题 (8分)同温同压下,同体积的氨气和硫化氢(H2S)气体的质量比为______________;同质量的氨气和硫化氢(H2S)气体的体积比为__________________,所含原子个数比为
_____________;若两者所含氢原子数相等,它们的物质的量比是__________________。
3、选择题 设NA为阿伏加德罗常数的值。下列说法正确的是
A.1 mol甲苯含有C―H键数目为8NA
B.1 mol丙烯酸中含有双键的数目为NA
C.由a g C2H4和C3H6组成的混合物中所含共用电子对数目为3aNA/14
D.在过氧化钠跟水的反应中,每生成2.24 L氧气,转移电子的数目为0.2NA
4、选择题 NA表示阿伏加德罗常数的值。下列叙述中不正确的是(?)
A.1mol乙烯与乙醇的混合物在氧气中充分燃烧,消耗氧气的分子数为一定为3NA
B.28g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA
C.常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA
D.常温常压下,22.4L氯气与足量镁粉充分反应,转移的电子数为2 NA
5、计算题 相对分子质量为M的某物质在室温下的溶解度为S g,此时测得饱和溶液的密度为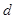 g/cm3,则该饱和溶液的物质的量浓度为?
g/cm3,则该饱和溶液的物质的量浓度为?