时间:2020-08-13 04:53:24
1、选择题 X元素最高氧化物对应的水化物为H3XO4,则它对应的气态氢化物为(?)。
A.HX
B.H2X
C.XH4
D.XH3
参考答案:D
本题解析:由X元素最高氧化物对应的水化物为H3XO4知X的最高价为+5,故其最低价为
―3价,对应氢化物为XH3,选D。
本题难度:简单
2、选择题 下列反应属于化合反应的是?
A.2Mg+O2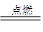 2MgO
2MgO
B.2Al+Fe2O3 A12O3+2Fe
A12O3+2Fe
C.CaCO3 CaO+CO2↑
CaO+CO2↑
D.KCl + Ag NO3 ="=" KNO3+AgCl↓
参考答案:A
本题解析:考查四种基本反应类型。两种或两种以上的物质化合生成一种物质的反应是化合反应,A正确。B是置换反应,C是分解反应,D是复分解反应。答案选A。
本题难度:一般
3、选择题 化学用语是学习化学的重要工具。以下化学用语表示错误的是
A.质量数之和是质子数之和两倍的水分子符号可能是:
B.NaHCO3水溶液呈碱性的原因:
C.基态硫离子的电子排布式:
D.熔融状态下硫酸氢钠的电离方程式: (熔融)=
(熔融)=
参考答案:B
本题解析:略
本题难度:一般
4、填空题 近年来地质、环境灾难频频发生,为防止在大灾之后疫病流行,灾区需要大量的各种消毒剂、漂白剂等。
(1)二氧化氯是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3与SO2在H2SO4作用下反应制得。请写出反应的离子方程式: 。
(2)过碳酸钠是一种新型固态漂白剂,化学式可表示为Na2CO3・3H2O2,它具有Na2CO3和H2O2的双重性质。过碳酸钠与下列物质均会发生化学反应而失效,其中过碳酸钠只发生了氧化反应的是 。
A.MnO2
B.KMnO4溶液
C.稀盐酸
D.Na2SO3溶液
(3)漂白剂亚氯酸钠(NaClO2)在常温下黑暗处可保存一年,HClO2不稳定可分解,反应的离子方程式为HClO2
参考答案:
本题解析:
本题难度:一般
5、填空题 (13分)近年来,我国对储氢纳米碳管的研究获得了重大进展,电弧法合成的纳米碳管常伴有大量物质――碳纳米颗粒。这种碳纳米颗粒可用氧化法提纯。其反应的化学方程式为:
C + K2Cr2O7+ H2SO4(稀)="=" CO2+ K2SO4+ Cr2(SO4)3+
(1)完成并配平上述反应的化学方程式。
(2)此反应的氧化剂是 ,氧化产物是 。
(3)H2SO4在上述反应中表现出来的性质是 。
A.酸性
B.氧化性
C.吸水性
D.脱水性
(4)上述反应中若产生11.2 L(标准状况下)的气体物质,则转移的电子数目为 。
参考答案:(13分)(1)3C+2K2Cr2O7+8H2SO4===3CO2+2K2SO4+2Cr2(SO4)3+8H2O(3分)
(2)K2Cr2O7 CO2(各2分) (3)A (3分) (4)1.204×1024(3分)
本题解析:根据化合价升降法可配平氧化还原反应方程式,反应中C的化合价升高氧化产物为CO2,K2Cr2O7 中Cr元素化合价降低,K2Cr2O7为氧化剂;H2SO4在反应中化合价没变,只表现出了酸性;根据配平后的方程式,生成3mol气体时转移12mol电子,当生成标况下11.2 L气体时,转移电子11.2L/22.4L/mol/3×12mol=2mol,即1.204×1024个电子。
考点:氧化还原反应方程式的配平及计算
本题难度:一般