时间:2020-07-28 06:02:27
1、选择题 A、B、C、D都是短周期元素,原子半径:D>C>A>B.已知A、B同周期,A、C同主族,C原子核内的质子数等于A、B原子核内的质子数之和,C原子最外层电子数是D原子最外层电子数的3倍.下列说法中正确的是( )
A.B、C、D三种元素组成的化合物的化学式为D2CB2
B.A、C两元素处在元素周期表中的第ⅥA族
C.B、C、D三种元素的简单离子的半径大小顺序为:C>D>B
D.B、D两元素可形成两种离子化合物,其阴、阳离子数之比均为1:2
参考答案:A、B、C、D都是短周期元素,根据原子半径D>C>A>B,且A、B同周期,A、C同主族,推知A、B、C、D在周期表中的大致相对位置为: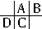
,C原子序数等于A原子序数+8,C原子核内的质子数等于A、B原子核内的质子数之和,故B原子序数为8,故B为氧元素.
C原子最外层电子数是D原子最外层电子数的3倍,若D的最外层电子数为1,则C为铝元素,A为硼元素,D为钠元素;若D的最外层电子数为2,则C为硫元素,A为氧元素,不合题意.
所以A为硼元素,B为氧元素,C为铝元素,D为钠元素.
A、B为氧元素,C为铝元素,D为钠元素,B、C、D三种元素组成的化合物的化学式为NaAlO2,故A错误;
B、A为硼元素,C为铝元素,最外层电子数都为3,两元素处在元素周期表中的第ⅢA族,故B错误;
C、B、C、D三种元素的简单离子分别为O2-、Al3+、Na+,三种离子核外电子排布相同,核电核数越大,离子半径越小,则有O2->Na+>Al3+,故C错误;
D、B为氧元素,D为钠元素,B、D两元素组成的离子化合物Na2O、Na2O2中阴、阳离子的个数比都为1:2,故D正确.
故选D.
本题解析:
本题难度:简单
2、选择题 下列过程中,共价键被破坏的是
[? ]
A.碘升华
B.溴蒸气被木炭吸附
C.酒精溶于水
D.HCl气体溶于水
参考答案:D
本题解析:
本题难度:简单
3、选择题 X、Y、Z、W为四种短周期主族元素.其中X、Z同族,Y、Z同周期,W与X、Y既不同族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高正价与最低负价的代数和为6.下列说法正确的是( )
A.Y元素最高价氧化物对应水化物的化学式为H2YO4
B.原子半径由小到大的顺序为:W<X<Z<Y
C.X与W可以形成W2X、W2X2两种氧化物
D.Y、Z两元素的气态氢化物中,Z的气态氢化物稳定
参考答案:C
本题解析:
本题难度:简单
4、选择题 下列有关化学键与晶体结构说法正确的是( )
A.两种元素组成的分子中一定只有极性键
B.离子化合物的熔点一定比共价化合物的高
C.非金属元素组成的化合物一定是共价化合物
D.含有阴离子的化合物一定含有阳离子
参考答案:D
本题解析:
本题难度:一般
5、选择题 下列物质中含有极性共价键的是?
[? ]
A.单质碘?
B.氯化镁?
C.溴化钾?
D.水
参考答案:D
本题解析:
本题难度:简单