时间:2020-07-28 06:01:25
1、简答题 为了探究HClO的漂白性,某同学设计了如下的实验.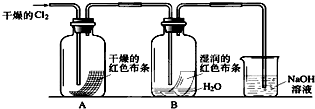
(1)通入Cl2后,从集气瓶A中干燥的红色布条的现象可得出的结论是______;从集气瓶B中湿润的红色布条的现象可得出的结论是______,其中发生的反应的化学方程式为______.
(2)为了确证是HClO使湿润的红色布条褪色,你认为还应增加的实验是______.
(3)烧杯中溶液所起的作用是______,烧杯中所发生反应的化学方程式为______.
(4)为保证实验安全,当氯气以每分钟1.12L(标准状况)的流速匀速通入时,若实验需耗时4分钟,小烧杯中盛2mol?L-1的NaOH溶液的体积至少应为______mL.
2、选择题 下列气体,溶于水后可以生成两种酸的是( )
A.潮湿的氯气通过盛有浓H2SO4的洗气瓶
B.碳与浓H2SO4加热反应
C.浓H2SO4使木条变黑
D.实验室用浓H2SO4制HCl其方程式:2NaCl+H2SO4(浓)
3、选择题 四支试管分别充满O2、NO2、Cl2、NH3四种气体,把它们分别倒立于盛有下列各种液体的水槽中,发生的现象如下图所示,其中充满Cl2的试管是
[? ]
A.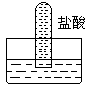
B.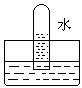
C.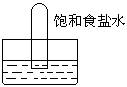
D.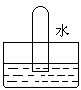
4、选择题 织物漂白剂亚氯酸钠(NaClO2)在溶液中可生成ClO2,HClO2,ClO2-,Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2是有毒气体。某温度下,各组分含量随pH变化情况如图所示(Cl-没有画出)。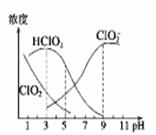
下列说法正确的是 ( ?)
A.NaClO2溶液中,c(Na+)/c(ClO2-)=1
B.往NaClO2溶液中滴入稀盐酸,当pH>6时,溶液中主要反应的离子方程式是:ClO2-+H+=HClO2
C.使用该漂白剂的最佳pH为3.0
D.此温度下HClO2的电离平衡常数的数值Ka=10-6
5、选择题 将下列物质分别加入溴水中,溴水颜色不变浅的是( )?
A.KCl晶体
B.H2 S气体?
C.CCl4
D.Mg