时间:2020-07-28 05:47:36
1、简答题 用含有A12O3、SiO2和少量FeO・xFe2O3的铝灰制备A12(SO4)3・18H2O。工艺流程如下: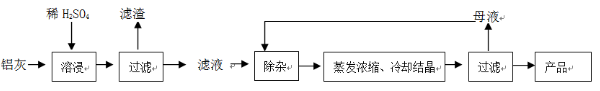 ?
?
(一定条件下,MnO4- 可与Mn2+反应生成MnO2)
已知: 生成氢氧化物沉淀的pH
| ? | Al(OH)3 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀时 | 3.4 | 6.3 | 2.7 |
| 完全沉淀时 | 5.2 | 9.7 | 3.2 |
参考答案:(1)Al2O3+6H+=2Al3++3H2O
(2)取少量滤液,滴加KMnO4溶液,KMnO4溶液褪色
(3)①将Fe2+氧化为Fe3+;调节pH值使铁完全沉淀;
②有黄绿色气体生成;MnO2+4HCl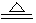 ?MnCl2+ Cl2↑+2H2O
?MnCl2+ Cl2↑+2H2O
③除去过量的MnO4-。
(4)K2SO4。
本题解析:(1)硫酸溶解氧化铝生成硫酸铝和水,反应的离子方程式为:Al2O3+6H+=2Al3++3H2O;
(2)取少量滤液,滴加KMnO4溶液,KMnO4溶液褪色。
(3)①将Fe2+氧化为Fe3+,调节pH值使铁完全沉淀;
②加入浓盐酸与MnO2反应生成有黄绿色气体;MnO2+4HCl= MnCl2+ Cl2↑+2H2O
③MnO4-可与Mn2+反应生成MnO2,过滤除去,所以可以利用MnSO4的溶液和高锰酸钾溶液反应生成二氧化锰,把过量高锰酸根离子除去。
(4)多次循环的物质是K2SO4。
本题难度:一般
2、选择题 工业上制造镁粉是将镁蒸气在气体中冷却.可作为冷却气体的是( )
①空气? ②CO2 ? ? ③Ar? ?④H2? ?⑤N2.
A.①②
B.②③
C.③④
D.④⑤
参考答案:C
本题解析:
本题难度:简单
3、选择题 铝热剂中铝的作用是
[? ]
A.催化剂
B.氧化剂
C.还原剂
D.填充剂
参考答案:C
本题解析:
本题难度:简单
4、填空题 如图所示,把试管小心地放入盛有(20 ℃)碳酸饮料的烧杯中,试管中开始放入几小块镁片,再用滴管滴加5mL稀盐酸于试管中。试回答下列问题
(1)实验中观察到的现象是
①镁片上有大量气泡产生;②镁片逐渐溶解;③_______________________。
(2)产生上述现象的原因是_______________________
(3)由实验推知,MgCl2溶液和氢气的总能量______________(填“大于”“小于”或“等于”)镁片和盐酸的总能量。
参考答案:(1)③烧杯中液体放出气泡的速率加快
(2)镁与稀盐酸反应产生H2,该反应为放热反应,碳酸饮料中CO2气体在水中的溶解度随温度升高而减小,故烧杯中液体放出气泡的速率逐渐加快
(3)小于
本题解析:
本题难度:一般
5、选择题 将镁粉加入FeCl3溶液中,可观察到的现象是①有气泡产生;②有红褐色沉淀产生;③镁粉逐渐溶解,溶液由黄色逐渐变成浅绿色;其中正确的是(? )
A.①
B.①②
C.①③
D.①②③
参考答案:D
本题解析:Fe3++3H2O Fe(OH)3+3H+,Mg+2H+====Mg2++H2↑,加入Mg粉能促进Fe3+水解,生成Fe(OH)3沉淀,故D选项正确。
Fe(OH)3+3H+,Mg+2H+====Mg2++H2↑,加入Mg粉能促进Fe3+水解,生成Fe(OH)3沉淀,故D选项正确。
本题难度:简单