ʱ��:2020-07-28 05:29:36
1��ѡ���� ����ϩ��C2H4������ȩ(C2H4O)��ɵĻ�����壬���ⶨ����̼������������72���������������������������ǣ�
A��36.36��
B��22.22%
C��16.00%
D��12.00%
�ο��𰸣�C
�����������
�����Ѷȣ���
2��ѡ���� ����ʵ�������ȷ���ǣ�?��
A���ڴ������ڵ������£�������ˮ������Ӧ��������ɫ��ˮ�ص�Һ���屽
B�����Թ����ȼ���һ����Ũ���ᣬ�����μ�������Ũ����ͱ���Ȼ�������ȡ������
C��ʵ������ȡ��Ȳʱ���ñ���ʳ��ˮ��������ˮ���Եõ�ƽ�ȵ�����
D����֤������ˮ�����ʱ���������������������Һ��ϣ��������Һ�����ã���Һ��ֲ�μ���������Һ
�ο��𰸣�C
���������A����Fe�������������£�����Һ�巢��ȡ����Ӧ��������ɫ��ˮ�ص�Һ���屽������B�����Թ����ȼ���һ����Ũ����Ȼ���ټ�������Ũ���ᣬ��������ȡ�����ȴ������ʱ�ټ��뱽��Ȼ��ˮԡ������ȡ������������C��ʵ�����õ�ʯ��ˮ��Ӧ��ȡ��Ȳʱ����Ӧ���ʺܿ졣Ϊ�˵õ�ƽ�ȵ��������ñ���ʳ��ˮ��������ˮ������εμӣ������ƻ�ѧ��Ӧ���ʡ���ȷ��D������������Br����ԭ�ӵ���ʽ���ڵġ���֤������ˮ�����ʱ���������������������Һ��ϼ��ȣ��������Һ�����ã���Һ��ֲ��ȡ�ϲ���Һ�����������ữ���ٵμ���������Һ�����е���ɫ�������ɣ���֤�������鷢����ˮ�ⷴӦ������
�����Ѷȣ�һ��
3������� ����10�֣���֪ij�л�����n(C): n(H)="1," ��W1g���л��������������г��ȼ�գ����ı�״���µ�����V L������ֻ��CO2��H2O����m(CO2)=w2g��m(H2O)=W3g��
��1����ͨ��������ȷ�����л����Ƿ���������֪��̼��ԭ�Ӹ������⣬�����������������е��������������⼸�����ݵ���Ϲ����������֣�����Щ���һһ�������пո��С�
����˵������ѡ��V��W1��W2��W3��ʾ�������г��������ʽ��
������������ÿ���ո�����һ����ϣ��м�����Ͼ���֣�����������
| ? | ? | ? | ? |
| ? | ? | ? | ? |
�ο��𰸣�
��1��2����5
W1��W2
W?1��W3
W?3?��V
W1��V
W2��V
?
?
?
����дһ��������1�֣�
��2��V��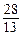 W1��������V��
W1��������V��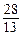 W1
W1
��3��W1��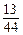 W2
W2
�����������
�����Ѷȣ���
4��ѡ���� ����Ȳ����ȩ��ɵĻ�����壬���ⶨ����̼������������72���������������������������ǣ�?��
A��32.33��
B��22.65%
C��19.56%
D��2.14%
�ο��𰸣�C
�����������ȲΪC2H2����ȩΪC2H4O---C2H2(H2O)��CH��̼���Ϊ12:1��̼������������72���������������Ϊ6����H2O���ܺ���Ϊ22����������������Ϊ22����16��18=19.56����
�����Ѷȣ�һ��
5��ʵ���� ��10�֣���ȩ������ͭ�������ڵ������£����Ա��������������ᡣ���ݴ�ԭ�����ʵ���Ƶò����Թ�C���ռ�������������Һ����ͼ��ʾ���Թ�A��װ��40������ȩˮ��Һ������ͭ��ĩ���Թ�C��װ����������ˮ���ձ�B��װ��ijҺ�壩����֪��60�桫80��ʱ��˫�����������������ɷ�����ȩ��������Ӧ����������ʮ���η�Ӧ������ȫ���й����ʵķе���±���
| ���� | ��ȩ | ���� | ���� | �Ҷ��� | ˮ |
| �е� | 20.8�� | 117.9�� | 290�� | 197.2�� | 100�� |

�ο��𰸣���1��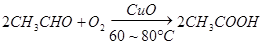 ?��2�֣�
?��2�֣�
��2���Թ�A�ķ�ӦҺ�У�1�֣�������Ӧ��Һ���¶ȣ�1�֣�?�Թ�A��֧�ܿڴ���1�֣�?�ռ����������֣�1�֣�
��3��ʹ�Թ�A�ڵķ�ӦҺ�������ȷ�����Ӧ��ʹ���ɵ����������������Թ�C��1�֣�?�Ҷ�������ͣ�ֻдһ������1�֣�
��4������һ��������̼�����Ʒ�δ������һ���ྻ���Թ��У����������Թ�C�е�Һ�壬���������������˵���Թ�C�к��в������ᡣ
����������һ��pH��ֽ���ڱ�������Ƭ���ϣ��ýྻ������IJ�����պȡ�Թ�C�ڵ�Һ�壬����pH��ֽ�в�����ֽ��ɫ���ñ���ɫ���Ƚ���ȷ����Һ��pH������˵���Ƿ����������ɣ��𰸺�������ȷ������2�֣�
�����������1������C���ռ������������֪����ȩ������ֱ���������ᣬ����ʽΪ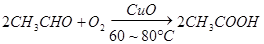 ��
��
��2����ʼ�Σ���ȩ����������Ӧ��������Ҫ������ӦҺ���¶ȣ����¶ȼƵ�ˮ����Ӧ�����Թ�A�ķ�ӦҺ�С�����Ӧ����֮����Ҫ���������������������������¶ȣ������Ҫ��ˮ��������Թ�A��֧�ܿڴ���
��3��B��������ʹ�Թ�A�ڵķ�ӦҺ�������ȷ�����Ӧ��ʹ���ɵ����������������Թ�C����������ķе���117.9�棬����B�е�Һ��ķе�������117.9�棬���Կ�ѡ����ͻ��Ҷ�����
��4�����Ậ���Ȼ������ԣ��������ͨ�ԣ����Ժ�̼�����Ʒ�Ӧ����CO2���塣����ͨ���������ڵ�pH����֤��
�����Ѷȣ�һ��