时间:2020-07-28 04:44:04
1、简答题 下表为元素周期表的一部分,请参照①~⑩在表中的位置,用化学用语回答下列问题: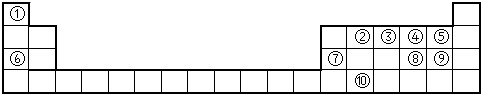
(1)元素③形成的单质的电子式为______;元素②形成的最高价氧化物的结构式为______.
(2)⑥、⑦两元素的最高价氧化物的水化物之间反应的离子方程式为______.
(3)②、③、④、⑤元素形成的氢化物中,热稳定性最强的是______(填化学式),沸点最高的是______(填化学式).
(4)⑧、⑨元素的最高价氧化物的水化物酸性强弱比较______(填化学式).
(5)元素⑩在周期表中的位置______;该元素的单质主要用途______(选填一种).
参考答案:(1)表中③是N,N2的电子式是
;②是C,其最高氧化物是CO2,其结构式为O=C=O,故答案为:
;O=C=O;
(2)⑥、⑦分别是Na、Al,其最高价氧化物的水化物分别是NaOH和Al(OH)3,二者反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O,故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(3)②、③、④、⑤分别是C、N、O、F,根据同周期从左到右元素氢化物稳定性逐渐增强可知,稳定性最强的是HF,沸点最高的应该是H2O,因为在这几种元素的氢化物中只有H2O在常温下是液体,其余是气体(也可从氢键解释),故答案为:HF;H2O;
(4)⑧、⑨分别是S、Cl,根据同周期最高价氧化物的水化物从左到右酸性逐渐增强可知,酸性为:HClO4>H2SO4,故答案为:HClO4>H2SO4;
(5)⑩是Ge,处于周期表中的第4周期ⅣA族,与Si一样可做半导体材料,故答案为:第4周期ⅣA族;半导体材料.
本题解析:
本题难度:一般
2、选择题 下列关于物质性质变化的比较,正确的是( )
A.非金属性强弱:C>Si>P
B.原子半径大小:Na>S>O
C.金属性性强弱:Mg>Na>Li
D.还原性强弱:F->Cl->I-
参考答案:A、同主族元素的单质从上到下,非金属性减弱,所以C>Si,同周期元素的单质从右到左,非金属性减弱,所以Si<P,故A错误;
B、同主族元素的单质从上到下,原子半径逐渐增大,所以S>O,同周期元素的单质从左到右,原子半径逐渐减小,所以Na>S,即Na>S>O,故B正确;
C、同主族元素的单质从上到下,金属性增强,所以Na>Li,同周期元素的单质从右到左,金属性增强,所以Mg<Na,故C错误;
D、元素单质氧化性氟气>氯气>单质碘,则离子的还原性顺序:F-<Cl-<I-,故D错误.
故选B.
本题解析:
本题难度:一般
3、选择题 下列各组无机酸的酸性强弱比较正确的是
A.HClO>HClO2>HClO3>HClO4
B.HF
参考答案:B
本题解析:
本题难度:简单
4、选择题 按C、N、O、F的顺序,下列递变规律正确的是( )
A.原子半径逐渐增大
B.元素原子得电子能力逐渐减弱
C.气态氢化物稳定性逐渐增强
D.最高化合价逐渐增高
参考答案:C、N、O、F在周期表相同周期,从左到右原子序数逐渐增大,则
A.同周期元素从左到右原子半径逐渐减小,故A错误;
B.同周期元素从左到右元素的非金属性逐渐增强,得电子能力逐渐增强,故B错误;
C.同周期元素从左到右元素的非金属性逐渐增强,对应的气态氢化物稳定性逐渐增强,故C正确;
D.F的最高化合价为0价,无正价,故D错误.
故选C.
本题解析:
本题难度:一般
5、选择题 国际无机化学命名委员会在1989年作出决定,把长式元素周期表原先的主、副族及族号取消,由左至右改为18列,如碱金属元素为第1列,稀有气体元素为第18列。按此规定,下列说法中不正确的是
[? ]
A.第15列元素的最高价氧化物为R2O5
B.第2列元素中肯定没有非金属元素
C.第17列元素的第一种元素无含氧酸
D.第16、17列元素都是非金属元素
参考答案:D
本题解析:
本题难度:简单