时间:2020-07-28 04:10:52
1、填空题 常温下,将0.01molCH3COONa和0.004molHCl溶于水,配制成0.5L混合溶液。判断:
(1)溶液中共有______________种微粒。
(2)溶液中有两种微粒的物质的量之和一定等于0.01mol,它们是______________和______________。
(3)溶液中n(CH3COO-)+n(OH-)-n(H+)=______________mol。
参考答案:(1)7?(2)CH3COOH和CH3COO-?(3)0.0060
本题解析:(1)Na+、H+、Cl-、CH3COO-、OH-、H2O、CH3COOH;(3)n(Cl-)+n(CH3COO-) +n(OH-)=n(H+)+n(Na+)(电荷守恒),n(CH3COO-)+n(OH-)-n(H+)=n(Na+)-n(Cl-)="0.0060" mol。
本题难度:简单
2、选择题 在氨水中存在下列电离平衡:NH3・H2O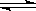 NH+OH-,下列情况能引起电离平衡向正向移动的有 ( )
NH+OH-,下列情况能引起电离平衡向正向移动的有 ( )
①加NH4Cl固体 ②加NaOH溶液 ③加HCl
④加CH3COOH溶液 ⑤加水 ⑥加热煮沸
A.①③⑤
B.①④⑥
C.③④⑤
D.①②④
参考答案:C
本题解析:加入NH4Cl固体c(NH4+)增大,平衡逆向移动,加NaOH溶液c(OH-)增大,平衡逆向移动,加HCl, c(OH-)减小,平衡正向移动,加CH3COOH溶液,c(OH-)减小,平衡正向移动,加水平衡正向移动,加热氨气挥发,平衡逆向移动,所以答案选C。
考点:影响电离平衡的因素
点评:改变影响平衡移动的一个因素,平衡总是向减弱这种改变的方向移动。
本题难度:一般
3、选择题 在氨水中存在下列电离平衡:NH3・H2O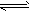 NH4++OH-,下列情况能引起电离平衡向正向移动的有
NH4++OH-,下列情况能引起电离平衡向正向移动的有
[? ]
①加NH4Cl固体 ②加NaOH溶液 ③加HCl ④加CH3COOH溶液 ⑤加水 ⑥加压
A.①③⑤
B.①④⑥
C.③④⑤
D.①②④
参考答案:C
本题解析:
本题难度:一般
4、填空题 (6分)在稀氨水中存在平衡:NH3+H2O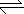 NH
NH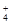 +OH-,如进行下列操作,则NH3、NH
+OH-,如进行下列操作,则NH3、NH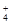 、H+、OH-浓度如何变化?请用“增大”“减小”“不变”填写。
、H+、OH-浓度如何变化?请用“增大”“减小”“不变”填写。
(1)通适量HCl气体时,c (NH3) ,c (H+) 。
(2)加入少量NaOH固体时,c(NH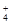 ) ,c (OH-) 。
) ,c (OH-) 。
(3)加入NH4Cl晶体时,c (NH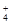 ) ,c (OH-) 。
) ,c (OH-) 。
参考答案:(1)、减小、增大 (2)、减小、增大 (3)、增大、减小
本题解析:(1)向氨水中通适量的氯化氢气体,氯化氢溶于水电离出氢离子,氢离子和氢氧根离子反应生成水,导致平衡正向移动,则溶液中氨气浓度减小,溶液的碱性减弱,所以溶液中氢原子浓度增大;(2)向氨水中加入少量NaOH固体,NaOH溶于水电离出氢氧根离子,氢氧根离子浓度增大,导致平衡逆向移动,则溶液中铵根离子浓度减小;(3)向氨水中加入氯化铵,氯化铵电离出铵根离子,所以溶液中铵根离子浓度增大,平衡逆向移动,从而抑制氨水电离,溶液中氢氧根离子浓度减小。
考点:考查弱碱的电离平衡。
本题难度:一般
5、选择题 对于常温下pH=3的乙酸溶液,下列说法正确的是( )
A.C(H+)=c(CH3COO-)+c(OH-)
B.加水稀释到原体积的10倍后溶液pH变为4
C.加入少量乙酸钠固体,溶液pH降低
D.与等体积pH=11的NaOH溶液混合后所得溶液中:c(Na+)=c(CH3COO-?)
参考答案:A、常温下pH=3的乙酸溶液,存在电荷守恒为:C(H+)=c(CH3COO-)+c(OH-),故A正确;
B、加水稀释到原体积的10倍后溶液pH变为4,但乙酸是弱电解质存在电离平衡,稀释促进电离,溶液又电离出氢离子,浓度增大,溶液PH小于4,故B错误;
C、乙酸钠溶于水溶液中的乙酸根离子抑制乙酸的电离,平衡左移,氢离子浓度减小,溶液PH增大,故C错误;
D、pH=3的乙酸溶液与等体积pH=11的NaOH溶液混合后所得溶液中是醋酸钠和醋酸的混合溶液:c(Na+)<c(CH3COO-?)故D错误;
故选A.
本题解析:
本题难度:简单