ʱ��:2020-07-28 03:55:53
1��ʵ���� ����ͼ�Ǽ�ͬѧ��Ƶ�֤��CO���л�ԭ�Ե�ʵ��װ�á�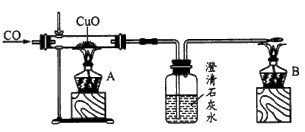
�ش��������⣺
(1)ʵ��ʱӦ�ȵ�ȼ___���A����B�������ľƾ��ơ�
(2)ϴ��ƿ�е�����Ϊ________��
(3)�ƾ���B��������____��
(4)��ͬѧ��������̫���ӣ��ɽ��ƾ��ƺ϶�Ϊһ��ȥ��B ����β�����ܿ���ת��A�Ļ����ϼ��ɣ���ͬѧ����Ƿ������____��������________��
(5)��ͬѧ����CO�ܷ�ʹ����ʯ��ˮ����ǣ�����������COͨ��CuO֮ǰӦ��ͨ������ʯ��ˮ���ų�CO�����ʯ��ˮ��Ӧ���ԶԴ��������ۣ�����Ϊ�������____ �����Ҫ������Ҫ����������________��
(6)��ͬѧ��Ϊ����Ƶ�װ����β����������������������������Ϊ��ͬѧ���һ�ֺ�����β������������___��
�ο��𰸣�(1)B
(2)����ʯ��ˮ�����
(3)��δ��Ӧ��COת��ΪCO2����ֹ��Ⱦ����
(4)������ ��A��B����ͬʱ��ȼ
(5)����Ҫ ���ڵ�ȼA֮ǰCO��ͨ������ʯ��ˮ
(6)�ڵ���ĩ����һ���ң�������ƿ���ٴ���
���������
�����Ѷȣ�һ��
2������� ��������ƣ�Na2S2O3���ɿ�����һ��Sԭ��ȡ����Na2SO4�е�һ��Oԭ�Ӷ��γɣ�ijУ��ѧ�о���ѧϰС���������ѧϰ��˼�룬ͨ��ʵ��̽��Na2S2O3�Ļ�ѧ���ʣ�
��������⡿Na2S2O3�Ƿ���Na2SO4���ƴӶ��߱����������أ�
����٣�______��
����ڣ���Һ�����ԣ��Ҳ����ᷴӦ��
����ۣ���ԭ�ԣ����ܱ�������������
��ʵ��̽����������������ڡ��ۣ����ʵ�鷽����
| ʵ����� | ʵ�������Ԥ��ʵ������ | ������ͣ������ӷ���ʽ��ʾ�� A��______ ��ҺpH=8 ����� ��pH=2�������еμ�Na2S2O3��Һ B��______ S2O32-+2H+�TS��+S02��+H2O ����� ��������ˮ��pH��2���еμ�����Na2S2O3��Һ ��ˮ��ɫ��dz C��______ |
�ο��𰸣���������⡿
���������Ȼ�����Ӧ���ɰ�ɫ����������Na2S2O3��BaCl2��Һ��Ӧ�г������ɣ�
�ʴ�Ϊ����BaCl2��Һ��Ӧ�г������ɣ�
��ʵ��̽����
A����������ˮ��Ĺ��ɣ�������ˮ�⣬������ˮ�⣬Խ��Խˮ�⣬˭ǿ��˭�ԣ�Na2S2O3Ϊǿ�������Σ�ˮ��ʼ��ԣ���PH��ֽ����Һ��PH��
�ʴ�Ϊ���ò�����պȡNa2S2O3��Һ����ε�pH��ֽ�����룬����ֽ���ֵ���ɫ�����ɫ�����գ�
B����pH=2�������еμ�Na2S2O3��Һ����������ƺ����ᷴӦ���ɶ���������������ʣ�Na2S2O3+H2SO4=Na2SO4+S��+SO2��+H2O��
�ʴ�Ϊ���е���ɫ��������ɫ�̼�����ζ���������
C������������ԭ��Ӧ��ʵ�ʵ�ʧ�����غ㣬S2O32-��2SO42-��8e-��Cl2��2CI-��2e-������4molCl2����1molS2O32-���õ�8molCl-��2molSO42-�����ݵ���غ㣬��������Ӧ��10molH+������ԭ���غ㷴Ӧ����Ӧ��5molH2O�����ӷ���ʽΪ
S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+��
�ʴ�Ϊ��S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+��
���������ۡ�
��1����ˮ�ijɷ��к��������ӣ����Ժ�AgNO3��Һ��Ӧ������ɫ������
�ʴ�Ϊ������ȷ������ˮ��������ˮ��ͬ������Cl-��
��2�����������ʱҪ�ų�̼������Ӻ�����������ӵĸ��ţ����Լ����������ữ���Ȼ�����Һ������а�ɫ������������֤��������������ӣ���֮��û�У�
�ʴ�Ϊ��ȡ������Ӧ�����Һ�������е��������ữ���Ȼ�����Һ�����۲쵽�а�ɫ������������˵��Na2S2O3�ܱ���ˮ������
���������
�����Ѷȣ�һ��
3������� ��14�֣�ij��ȤС���ѧ������Mg��CO2��Ӧԭ�����Ʋ���ҲӦ����CO2��ȼ�գ�Ϊ��ȷ�������ɲ��ﲢ����ʵ����֤��ijͬѧ�������ͼ��ʾװ�ý���ʵ�飨��֪PdCl2�ܱ�CO��ԭ�õ���ɫ��Pd������ش��������⣺
��1��Ϊʹ��Ӧ�濪���ã������ͣ��������Ӧѡ����ͼ��ʾ?װ�ã�����ĸ���ţ���
��2��ʵ������ȡ������̼�������õ�ҩƷ��?�����ţ���
��ʯ��ʯ���ڴ����С�մ�18.4 mol��L��1���ᣬ��11.2mol��L��1���ᣬ������ˮ����ľ̿�ۡ�
��3����2װ���ڽ��з�Ӧ�����ӷ���ʽΪ?�����װ�������Բ�װ��ҩƷ��ȼ�ƾ���֮ǰ��װ��?�������ֱ�ţ��г���?����ʱ���ٵ�ȼ�ƾ��ơ�
��4������װ��6���к�ɫ������װ��4�в������壨ֻ��һ�����ʣ������������ʹ����ʯ��ˮ����ǵ�����ų��������������̼��Ӧ�Ļ�ѧ����ʽΪ?��
����װ��6����Һ����������װ��4�в������壨���������ʣ������������ʹ����ʯ��ˮ����ǵ�����ų��������������̼��Ӧ�Ļ�ѧ����ʽΪ?��
�ο��𰸣���1��C(2��)����2���٢ݢ�(2��)��
��3��HCO3-+H+ =CO2��+ H2O(2��)��5(1��)����ɫ����(1��)��
=CO2��+ H2O(2��)��5(1��)����ɫ����(1��)��
��4��2CO2+2Na= Na2CO3+CO(3��)��3CO2+4Na= 2Na2CO3+C
������д�� �����ȡ���ȼ������ȷ��(3��),
�����ȡ���ȼ������ȷ��(3��),
�����������
�����Ѷȣ���
4��ѡ���� �й����ʵļ��飬����˵����ȷ���ǣ�������
A����ij��Һ�еμ�AgNO3��Һ�����ɰ�ɫ������˵��ԭ��Һ�к���Cl-
B��ij�������ʹȼ�ŵ�ľ��Ϩ��˵����������CO2
C���������ᣬ�ų���ʹ����ʯ��ˮ����ǵ���ɫ��ζ�����壬��һ���Ǻ���CO32-
D����ij��Һ�еμ�BaCl2��Һ���а�ɫ����������˵��ԭ��Һ��һ������CO32-����SO42-
�ο��𰸣�A����ij��Һ�еμ�AgNO3��Һ�����ɰ�ɫ������˵��ԭ��Һ�к���Cl-����CO32-�����ӣ���A����
B��ij�������ʹȼ�ŵ�ľ��Ϩ��˵����������CO����CO2�е�����һ�֣���B����
C���������ᣬ�ų���ʹ����ʯ��ˮ����ǵ���ɫ��ζ�����壬����Һ�п��Ժ���̼������ӡ�̼��������ӡ�����������ӻ�����������������е�����һ�֣���C��ȷ��
D����ij��Һ�еμ�BaCl2��Һ���а�ɫ����������˵��ԭ��Һ�д���CO32-��SO42-��Ag+�е�����һ�֣���D����
��ѡC��
���������
�����Ѷȣ�һ��
5��ʵ���� ��ͼ��ʾ�����Թ�С�ĵط���ʢ��̼�����ϵ��ձ���(20��)�������Թ��з��뼸С��þƬ�����õιܵμ�5 mLϡ�������Թ��С��Իش��������⣺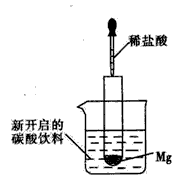
(1)ʵ���й۲쵽��������þƬ��____��þƬ���ܽ⣬�ձ���Һ��ų����ݵ����� ____����ӿ족�������������䡱����
(2)�������������ԭ����____��
(3)д���йط�Ӧ�����ӷ���ʽ��____��
(4)��ʵ����֪��MgCl����Һ��������������________������ڡ�����С�ڡ����ڡ���þƬ���������������
�ο��𰸣�(1)�д�������ð�����ӿ�
(2)þ��ϡ���ᷴӦ�ų��������÷�Ӧ��һ�����ȷ�Ӧ
(3)Mg+2H+==Mg2++H2��
(4)��
���������
�����Ѷȣ�һ��