时间:2020-07-08 01:42:39
1、简答题 氢氧化镁用于制药工业,还是重要的绿色阻燃剂.
I.治疗胃酸过多药物Stmoache的有效成分为Mg(OH)2.
(1)该药物治疗胃酸(主要成分为盐酸)过多症时反应的离子方程式为______;
II.已知:Mg(s)+2H2O(g)=Mg(OH)2(s)+H2(g)△H1=-441kJ?mol-1
H2O(g)=H2(g)+
| 1 2 |
| 1 2 |
| 精制阻燃剂的条件 | 阻燃剂铁含量 序号 提纯体系温度/℃ 加入EDTA质量/g 加入保险粉质量/g W(Fe)/(10-4g) 1 40 0.05 0.05 7.63 2 40 0.05 0.10 6.83 3 60 0.05 0.10 6.83 4 60 0.10 0.10 6.51 | |||
参考答案:(1)氢氧化镁和盐酸反应产生氯化镁和水,反应的离子方程式为Mg(OH)2+2H+=Mg2++2H2O,
故答案为:Mg(OH)2+2H+=Mg2++2H2O;
(2)Mg(s)+2H2O(g)=Mg(OH)2(s)+H2(g)△H1=-441kJ?mol-1 ①
H2O(g)=H2(g)+12O2(g)△H2=242kJ?mol-1②
Mg(s)+12O2(g)=MgO(s)△H3=-602kJ?mol-1③
方程式③+②-①得:Mg(OH)2(s)=MgO(s)+H2O(g);△H=81KJ/mol,
故答案为:Mg(OH)2(s)=MgO(s)+H2O(g);△H=81KJ/mol;
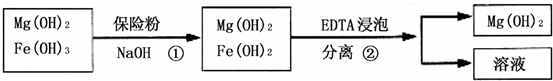
(3)每消耗0.1mol保险粉(Na2S2O4)转移0.6mol?e-,所以S2O42-被氧化为硫酸根离子,氢氧化铁被还原为氢氧化亚铁,发生的离子方程式为:6Fe(OH)3+S2O42-+2OH-=6Fe(OH)2+2SO42-+4H2O.
?故答案为:6Fe(OH)3+S2O42-+2OH-=6Fe(OH)2+2SO42-+4H2O;
(4)Fe(OH)2悬浊液中存在如下平衡:Fe(OH)2(s)=Fe2+(aq)+2OH-(aq)当不断滴入EDTA时,EDTA将结合Fe 2+促使平衡向右移动而使Fe(OH)2不断溶解.
故答案为:Fe(OH)2悬浊液中存在如下平衡:Fe(OH)2(s)=Fe2+(aq)+2OH-(aq)当不断滴入EDTA时,EDTA将结合
Fe 2+促使平衡向右移动而使Fe(OH)2不断溶解;
(5)观察实验2、3知,其它条件相同时,温度不同,铁含量相同,采取低温能抑制氢氧化镁的溶解,所以采用低温较好.
观察实验3、4知,其它条件相同时,EDTA质量越大,含铁量越低,所以选取EDTA质量为0.10g.
观察实验1、2知,其它条件相同时,保险粉质量越大,含铁量越低,所以选取保险粉质量为0.10g
故选C.
本题解析:
本题难度:一般
2、选择题 下列变化不可能通过一步实验直接完成的是( )
A.Al→Al(OH)3
B.MgO→Mg(OH)2
C.Fe(OH)3→Fe2O3
D.Ca2+→CaCO3
参考答案:A.由铝制备氢氧化铝至少需要两步才能完成,如Al→AlCl3→Al(OH)3,故A选;
B.氧化镁不能溶于水,不能通过一步反应直接完成MgO→Mg(OH)2的转化,故B选;
C.氢氧化铁在高温条件下发生分解产生Fe2O3,能一步实现,故C不选;
D.溶液中的钙离子和碳酸根离子反应,如Na2CO3+CaCl2=2NaCl+CaCO3↓,离子反应为:Ca2++CO32-=CaCO3↓,能一步实现,故D不选;
故选AB.
本题解析:
本题难度:简单
3、填空题 由铝土矿(主要成分是Al2O3)炼制铝的工艺流程示意图如下: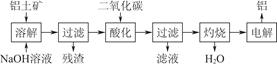
(1)电解生成的铝在熔融液的?(填“上层”或“下层”),电解时不断消耗的电极是?(填“阴极”或“阳极”)。
(2)写出通入过量二氧化碳酸化时反应的离子方程式?
?。
(3)电解制备铝时,需加入冰晶石(Na3AlF6),其作用是?,工业上可以用氟化氢气体、氢氧化铝和纯碱在高温条件下发生反应来制取冰晶石,写出该反应的化学方程式?。
(4)上述工艺所得铝中往往含有少量Fe和Si等杂质,可用电解方法进一步提纯,该电解池的阴极材料是?(填化学式),阳极的电极反应式为?。
(5)对金属制品进行抗腐蚀处理,可延长其使用寿命。
①控制一定条件进行电解(见图),此时铝表面可形成耐酸的致密氧化膜,其电极反应式为?;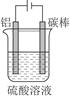
②钢材镀铝后,能防止钢材腐蚀,其原因是?。
参考答案:(1)下层 阳极
(2)AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
(3)助熔剂(或降低熔化温度)? 2Al(OH)3+12HF+3Na2CO3 2Na3AlF6+3CO2+9H2O
2Na3AlF6+3CO2+9H2O
(4)Al Al-3e-=Al3+
(5)①2Al-6e-+3H2O=Al2O3+6H+
②致密的氧化铝膜起着保护内部金属的作用,若镀层破损后,与电解质溶液接触时形成原电池,铝作负极防止钢材被腐蚀
本题解析:(1)电解熔融的氧化铝冶炼铝,阳极生成O2,与石墨电极反应生成CO。(3)氧化铝的熔点很高,是常用的耐高温材料,故冶炼时加入冰晶石降低其熔点。(4)迁移电解法精炼铜的原理,电解时铝在阴极析出,故阴极材料为纯铝。(5)根据题中信息,铝表面生成的应为Al2O3,故阳极电极反应为铝失去电子,生成的Al3+与H2O作用形成Al2O3。
本题难度:一般
4、填空题 某无色透明溶液,投入金属铝可放出H2。现有下列离子:Mg2+、Cu2+、Ba2+、H+、Ag+、SO42-、
HCO3-、OH-。试判断下列两种情况时,各有哪些离子可存在于此溶液中:
(1)当生成Al3+时,可存在的离子有?;
(2)当生成AlO2-时,可存在的离子有?。
参考答案:(1)H+、Mg2+、SO42-? (3分)(2)OH-、Ba2+(3分)
本题解析:略
本题难度:简单
5、填空题 (1)可以证明钠的硬度小的实验事实是__________________。
(2)可以说明自然界中不存在游离态的钠的实验事实是 _______________________________________________________________________________。
(3)可以证明氧化铝熔点高的实验事实是_______________________________________________________________________________________。
参考答案:(1)金属钠可以用普通刀片切割
(2)新切开的金属钠很快失去了光泽(被氧化)
(3)铝箔在酒精灯上加热没有液态的铝滴落
本题解析:
本题难度:一般