时间:2020-07-08 01:26:23
1、填空题 (1)与纯水的电离相似,液氨中也存在着微弱的电离:2NH3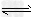 ?NH4++NH2-.据此判断,以下叙述错误的是 ( )
?NH4++NH2-.据此判断,以下叙述错误的是 ( )
A.液氨中含有NH3、NH4+、NH2-等粒子
B.一定温度下液氨中c(NH4+)・c(NH2-)是一个常数
C.液氨达到电离平衡时c(NH3)=c(NH4+)=c(NH2-)
D.只要不加入其他物质,液氨中c(NH4+)=c(NH2-)
(2)完成下列反应的化学方程式:
①在液氨中投入一小块金属钠,放出气体:__________________________________.
②NaNH2溶于水的反应:________________________________.
(3)类似于“H++OH-===H2O”的离子反应:_____________________________.
参考答案:(1)C
(2)①2Na+2NH3===H2↑+2NaNH2
②NaNH2+H2O===NaOH+NH3↑
(3)NH2-+NH4+===2NH3
本题解析:
本题难度:一般
2、选择题 已知室温时,0.1mo1/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是:
[? ]
参考答案:B
本题解析:
本题难度:一般
3、选择题 25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是
A.0.1mol/LCH3COONa与0.1mol/LHCl溶液等体积混合:c(Na+)=c(Cl-)>cCH3COO-)>c(OH-)
B.0.1mol/LNH4Cl与0.1mol/L氨水等体积混合(pH>7):c(NH3・H2O)>c(NH4+)>c(Cl-)>c(OH-)
C.0.1mol/LNa2CO3与0.1mol/L NaHCO3溶液等体积混合: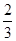 c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
D.0.1mol/LNa2C2O4与0.1mol/LHCl溶液等体积混合(H2C2O4为二元弱酸):
2c(C2O42-)+c(HC2O4-)+c(OH-)=c(Na+)+c(H+)
参考答案:AC
本题解析:A、0.1mol/LCH3COONa与0.1mol/LHCl溶液等体积恰好反应混合生成醋酸和氯化钠,醋酸电离溶液显酸性,则c(Na+)=c(Cl-)>cCH3COO-)>c(OH-),A正确;B、0.1mol/LNH4Cl与0.1mol/L氨水等体积混合(pH>7),这说明溶液显碱性,因此氨水的电离程度大于铵根的水解程度,则c(NH4+)>c(Cl-)>c(NH3・H2O)>c(OH-),B不正确;C、0.1mol/LNa2CO3与0.1mol/L NaHCO3溶液等体积混合,则根据物料守恒可知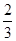 c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3),C正确;D、0.1mol/LNa2C2O4与0.1mol/LHCl溶液等体积混合(H2C2O4为二元弱酸),二者恰好反应生成草酸酸氢钠和氯化钠,则根据电荷守恒可知溶液中2c(C2O42-)+c(HC2O4-)+c(OH-)+c(Cl-)=c(Na+)+c(H+),D不正确,答案选AC。
c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3),C正确;D、0.1mol/LNa2C2O4与0.1mol/LHCl溶液等体积混合(H2C2O4为二元弱酸),二者恰好反应生成草酸酸氢钠和氯化钠,则根据电荷守恒可知溶液中2c(C2O42-)+c(HC2O4-)+c(OH-)+c(Cl-)=c(Na+)+c(H+),D不正确,答案选AC。
本题难度:一般
4、选择题 等质量的三份锌a、b和c,分别加入足量的稀硫酸中,a中同时加入适量CuSO4溶液,b中加入适量CH3COONa溶液,C中不加入其他物质.下列各图中表示其产生H2的总体积(V)与时间(t)的关系中正确的是( )
A.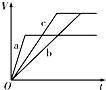
B.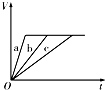
C.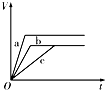
D.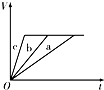
参考答案:锌和硫酸反应,加入硫酸铜,会置换出金属铜,形成锌、铜、稀硫酸原电池,加快金属铁和硫酸反应的速率,b中能生成醋酸,导致溶液中氢离子浓度减小,反应速率降低,所以反应速率是:a>c>b,则反应时间a<c<b;
生成氢气体积与加入锌的质量有关,a中部分锌和铜离子发生置换反应,则a中生成氢气最少,b、c中生成氢气相等,
故选A.
本题解析:
本题难度:简单
5、选择题 在-50 ℃时液氨中有2NH3(液)  NH4++NH2―电离平衡关系,两离子的平衡浓度均为1×10-15mol・L-1,下列对-50 ℃时液氨的电离平衡常数的表达中正确的是
NH4++NH2―电离平衡关系,两离子的平衡浓度均为1×10-15mol・L-1,下列对-50 ℃时液氨的电离平衡常数的表达中正确的是
A.电离平衡常数是1×10-15
B.不加入其他物质,液氨中c(NH4+)=c(NH2―)
C.降低温度,其电离平衡常数数值增加
D.此液氨中放入NH4Cl,其电离平衡常数的数值增加
参考答案:B
本题解析:电离平衡常数和化学平衡常熟类似,是生成物浓度的幂之积和反应物浓度放热幂之积的比值,A不正确。根据电离方程式可知B正确。电离是吸热放热,降低温度,电离平衡常数减小,C不正确。电离平衡常数只与温度有关系,D不正确。答案选B。
本题难度:一般