ʱ��:2020-07-08 01:22:10
1��ʵ���� ��14�֣�ij��ѧ��ȤС������ͼ��ʾװ�ý���̽��ʵ�飬����֤����������ϩ��������ϩ���в������ԡ����¶�Ѹ�������ɹ۲쵽�Թ�����ˮ��ɫ����ƿ��ŨH2SO4���Ҵ��Ļ��Һ���Ϊ�غ�ɫ��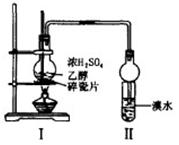
��д����ʵ����������ϩ�Ļ�ѧ����ʽ��
?
�Ƽ�ͬѧ��Ϊ�����ǵ��û��Һ�巴Ӧ�ĸ����ԣ���ˮ��ɫ��������֤����Ӧ������ϩ��������ϩ���в������ԣ���������ȷ����?������ĸ��ţ�
A����ϩ����ˮ����ȡ����Ӧ
B��ʹ��ˮ��ɫ�ķ�Ӧ��δ���Ǽӳɷ�Ӧ
C��ʹ��ˮ��ɫ�����ʣ�δ������ϩ
D��Ũ���������Ҵ�������ȩ��Ҳ��ʹ��ˮ��ɫ
����ͬѧ����ϸ�¹۲����Ϊ�Թ�����һ�����֤����Ӧ������ϩ���ɣ����������?
�ȱ�ͬѧ������ʵ��װ�ý����˸Ľ�����I��II֮��������ͼװ�ã���A�е��Լ�ӦΪ?����������?��B�е��Լ�Ϊ?��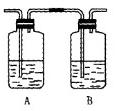
�ɴ�������ʵ�����ƿ�з�Һ����ȷ������?������ĸ��ţ���
A����Һ��ȴ������ˮ����
B����Һ��ȴ����շ�Һ����
C����ˮ������ƿ��ϡ�ͺ����Һ��
2��ѡ���� �����ܼ���ƾ����Ƿ���ˮ���Լ��ǣ�������
A������
B��������
C��̼���
D����ˮ����ͭ
3��ʵ���� ijУ��ѧ�о���ѧϰС����������˽�������ݣ��Ҷ���(HOOC-COOH���ɼ�дΪH2C2O4)�׳Ʋ��ᣬ������ˮ�����ڶ�Ԫ��ǿ��(Ϊ�������)��������ǿ��̼�ᣬ���۵�Ϊ101.5�棬��157��������Ϊ̽������IJ��ֻ�ѧ���ʣ�����������ʵ�飺
(1)��ʢ��1 mL����NaHCO3��Һ���Թ��м��������Ҷ�����Һ���۲쵽����ɫ���ݲ������÷�Ӧ�����ӷ���ʽΪ____________________________��
(2)��ʢ���Ҷ��ᱥ����Һ���Թ��е��뼸�������ữ��KMnO4��Һ������������Һ���Ϻ�ɫ��ȥ����˵���Ҷ������_____________(������ԡ�������ԭ�ԡ������ԡ�)��
������ƽ�÷�Ӧ�����ӷ���ʽ�� ____ MnO4- + ___ H2C2O4 + ____ H+ = ____ Mn2+ + ___ CO2�� + ____H2O
(3)��һ�������Ҷ�������Թ��У�����ͼ��ʾװ�ý���ʵ��(�г�װ��δ���)�� 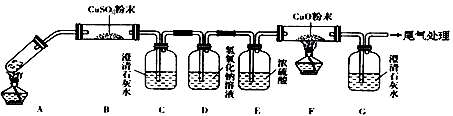
ʵ�鷢�֣�װ��C��G�г���ʯ��ˮ����ǣ�B��CuSO4��ĩ������F��CuO��ĩ��졣�ݴ˻ش�
������װ���У�D��������__________________�����Ҷ���ֽ�Ļ�ѧ����ʽΪ_____________________________________��
(4)��С��ͬѧ��2.52 g���ᾧ��(H2C2O4��2H2O)���뵽100 mL 0.2 mol/L��NaOH��Һ�г�ַ�Ӧ����÷�Ӧ����Һ�����ԣ���ԭ����___________________________________(�����ּ���)������Һ�и����ӵ�Ũ���ɴ�С��˳��Ϊ��___________________�������ӷ��ű�ʾ����
4������� ijͬѧ�����ͼװ�ã��о��ǽ���Ԫ�����ʱ仯���ɣ�
��1����֪���ᣨH2SiO3����һ��������ˮ�����ᣬ�ʰ�ɫ���ڻ�ѧ��Ӧ�У�һ��أ�ǿ���������ᣬ��NaHCO3+HCl�TNaCl+CO2��+H2O���ó���HCl����ǿ��H2CO3�����ԣ�����������Һ��̼��ơ�����ʯ��ˮ����������Һ��ѡ���Լ�����ͼװ��֤�������ԣ�HNO3��H2CO3��H2SiO3��
A��װ�Լ�______��B��װ�Լ�______��C��װ�Լ�______��C��ʵ������Ϊ______��д��C�з�����Ӧ�����ӷ���ʽ______��
��2����֪��������ڳ�������Ũ���ᷴӦ����������������ͼװ��֤������������ǿ�ڵⵥ�ʵ������ԣ���A��װŨ���ᣬB��װ�������ط�ĩ��C��װ�Լ�______��C������______��д�����ӷ���ʽ______����ʵ��װ�������Բ��㣬��ָ���Ľ�������______��
��3�����C��װ������������Һ��A��װŨ���ᣬB��װ���������Һ����Ӧ��ʼ��۲�������C�в�������ɫ������д����ѧ����ʽ______��֤���ȵķǽ����Ա���ķǽ�����______���ǿ�������������жϡ�����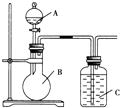
5��ѡ���� ��������ʵ���������ý��۴������ 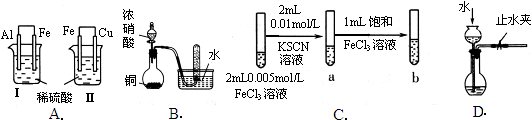
| ʵ�� | ʵ������ | ���� |
| A | ���ձ�����Ƭ���������ݣ����ձ���ͭƬ���������� | ��ԣ�Al��Fe��Cu |
| B | �Թ����ռ�����ɫ���� | ͭ��Ũ���ᷴӦ������NO |
| C | �Թ�b���Թ�a����Һ�ĺ�ɫ�� | ����Ӧ��Ũ�ȣ�ƽ��������Ӧ�����ƶ� |
| D | ����©����Һ�������ƿ��Һ���ұ��ֲ��� | װ������������ |