时间:2020-07-08 01:15:39
1、选择题 已知I-、Fe2+、SO2、Cl-和H2O2均有还原性,它们在酸性溶液中还原性的顺序为SO2>I->Fe2+>H2O2>Cl-,则下列反应不可能发生的是( )
A.2Fe3++SO2+2H2O===2Fe2++SO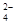 +4H+
+4H+
B.I2+SO2+2H2O===H2SO4+2HI
C.2Fe2++I2===2Fe3++2I-
D.H2O2+SO2===H2SO4
2、选择题 溶液中可发生以下反应:①16H++10Z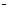 +2XO
+2XO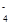 =2X
=2X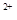 +5Z2+8H2O,②2M
+5Z2+8H2O,②2M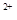 +R2=2M
+R2=2M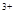 +2R-,③2R-+Z2=R2+2Z-由此判断下列说法错误的是
+2R-,③2R-+Z2=R2+2Z-由此判断下列说法错误的是
A.氧化性强弱: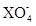 <Z2 <R2 <M
<Z2 <R2 <M
B.还原性强弱:X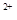 <Z
<Z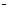 <R
<R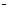 <M
<M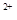
C.Z元素在反应①中被氧化,在③中被还原
D.常温下可发生反应2M2++Z2=2M3++2Z-
3、选择题 有一种酸性溶液中存在NO-3、I-、Cl-、Fe3+中的一种或几种离子,向该溶液中加入溴水,溴单质被还原,由此可推断溶液中( )
A.一定含有I-,不能确定是否有Cl-
B.一定含有NO-3
C.可能含有Fe3+
D.一定含有I-、NO-3和Cl-
4、简答题 类比是化学学习中常用的方法之一,已知硝酸能把铁氧化成Fe(NO3)3,但当铁过量时,产物是Fe(NO3)2.某同学受此启发,提出一个相似的观点:氯气与铁粉反应,当Cl2足量时生成FeCl3,当铁粉过量时产物是FeCl2.为验证此观点是否正确,该同学将一根细的纯铁丝分别在足量和少量的Cl2中点燃,取其表面生成物并分别编号为A、B,然后通过实验确定其成分.探究过程如下:
(1)提出假设:A是FeCl3,B是FeCl2.
(2)设计实验方案:分别取A、B的溶液均进行以下实验,但实验现象相同.请填写下表中的相应空格
| 实验方法 实验现象 | 结论 分别向A、B溶液中加KSCN溶液 ______ 固体物质中FeCl3 分别向KMnO4溶液中加入适量A、B溶液 KMnO4溶液颜色无明显变化 固体物质中不含______ |
5、选择题 已知?2Fe3++2I-=2Fe2++I2,2Fe2++Cl2=2Fe3++2Cl-,则有关离子的还原性由强到弱的顺序为( )
A.Cl->Fe2+>I-
B.Fe2+>I->Cl-
C.I->Fe2+>Cl-
D.Fe2+>Cl->I-