时间:2020-07-08 01:14:14
1、选择题 下列有关金属及其化合物的说法正确的是
[? ]
A.1 L生理盐水(0.9%NaCl溶液)中含有9 molNa+
B.镁条在空气中可以点燃而经过打磨的铁丝却不能,说明Mg比Fe还原性更强
C.实验室里可以用酚酞溶液来鉴别相同物质的量浓度的碳酸钠和碳酸氢钠溶液
D.节日燃放烟花时产生的黄色火焰色是因为在烟花里放入了钠单质
参考答案:BC
本题解析:
本题难度:简单
2、选择题 将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀与通入CO2的量的关系可表示为
[? ]
A.
B.
C.
D.
参考答案:C
本题解析:
本题难度:一般
3、选择题 把铝粉和某铁氧化物xFeO・yFe2O3粉末配成铝热剂,再分成两等份。一份在高温下恰好完全反应后,再与足量盐酸反应;另一份直接放入足量的烧碱溶液中充分反应。前后两种情况下生成的气体质量比是8:11,则x:y为?
A.5:7
B.7:5
C.1:2
D.2:3
参考答案:D
本题解析:设生成气体的质量为8g和11g,则根据第二份的实验,铝和烧碱反应生成气体为11g,则铝的物质的量为11/3 mol,而第一份中由于铝粉与铁的氧化物恰好完全反应,所以后面是置换出来的铁与盐酸反应生成的氢气,根据方程式计算,生成8g氢气,需要铁为4mol,而在铝热反应中,铝失电子,铁得电子,可以列出方程式为:
x+2y=4
11=x*2+2y*3
计算可得x=1,y=1.5,所以x:y=2:3
点评:本题结合铝热反应和铝与烧碱的反应,突破点在于先根据比值设一个具体数值来计算铝的物质的量,再根据氧化还原反应电子得失守恒来列方程式计算。
本题难度:简单
4、填空题 铝是一种应用广泛的金属,工业上用Al2O3和冰晶石(Na3AlF6)混合熔融电解制得。铝土矿的主要成分是Al2O3和SiO2及其它不溶于NaOH溶液的杂质。从铝土矿中提炼Al2O3的流程如下: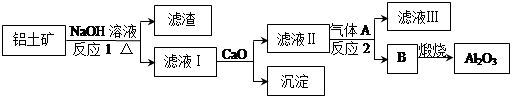
回答下列问题:
(1)写出反应1的化学方程式?;
(2)滤液Ⅰ中加入CaO生成的沉淀是?,反应2的离子方程式为?;
(3)电解制铝的化学方程式是?,以石墨为电极,阳极产生的混合气体的成分是?。
参考答案:(1)2NaOH+SiO2=Na2SiO3+H2O(2分) 2NaOH+Al2O3=2NaAlO2+H2O(2分)
(2)CaSiO3(1分)?
?2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-?或AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-(2分)
(3)2Al2O3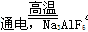 4Al+3O2↑(2分) ?O2、CO2(CO)(2分)
4Al+3O2↑(2分) ?O2、CO2(CO)(2分)
本题解析:(1)酸性氧化物、两性氧化物都能溶于强碱溶液,生成盐和水;(2)氧化钙是碱性氧化物,与水反应生成氢氧化钙,钙离子与硅酸根离子结合成硅酸钙沉淀;偏铝酸盐溶液通入少量或过量CO2,可以制取氢氧化铝沉淀;(3)电解熔融氧化铝可制取铝;阳极反应式为2O2――2e―=O2↑,高温下C与O2反应生成CO2或CO。
本题难度:一般
5、选择题 甲、乙两个烧杯中分别盛有100 mL 4.0 mol/L的盐酸和100 mL 4.0 mol/L NaOH溶液,向两个烧杯中均加入5.4 g铝粉,在相同状况下产生气体的体积比为? (? )
A.1:1
B.2:3
C.3:2
D.3:1
参考答案:B
本题解析:100 mL 4.0 mol/L的盐酸n(HCL)=0.4 mol ;100 mL 4.0 mol/L NaOH 溶液n(NaOH)=0.4 mol;5.4 g铝粉n(AL)= 0.2 mol ;
根据反应:2AL + 6HCL ===== 2ALCL3 + 3H2↑可得AL过量;则
0.4 mol?0.2 mol
根据反应:2AL+2NaOH+2H2O=2NaALO2+3H2↑可得NaOH过量;则
0.2 mol?0.3 mol
所以正确答案为B
本题难度:简单