时间:2020-07-08 00:54:44
1、选择题 (山东诸城一中2009届高三年级阶段性评估,化学,15)下列各图所示装置的气密性检查中,漏气的是?
 |
参考答案:C
本题解析:C项中向外拉活塞,使锥形瓶内的压强减小,由于外界大气压的作用,长颈漏斗的导管下端的液柱应下降或锥形瓶中液体中产生气泡。故C装置气密性漏气。
本题难度:一般
2、实验题 (10分)蛇纹石是一种含水的富镁硅酸盐矿物的总称,可以看作由MgO、Fe2O3、Al2O3、SiO2组成。实验室以蛇纹石为原料制取水合碱式碳酸镁,已知:
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀的pH | 1.5 | 3.3 | 9.4 |
| 完全沉淀的pH | 3.7 | 5.2 | 11.0 |
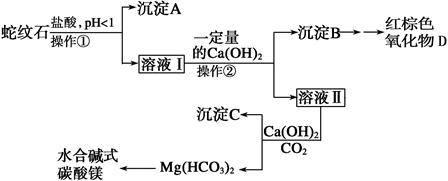
参考答案:⑴玻璃棒、漏斗、烧杯?(2分)?⑵ C(2分)
⑶取少量溶液Ⅱ于试管中,加入KSCN溶液,若无明显现象,说明溶液Ⅱ不含Fe3+;若溶液变红色,说明溶液Ⅱ含有Fe3+。?(2分)
⑷ OH-+Al(OH)3 = AlO2-+2H2O (2分)? ?过滤、加热或灼烧(2分,每个1分)
本题解析:(1)操作①是过滤,所以需要的玻璃仪器是玻璃棒、漏斗、烧杯。
(2)操作②的目的是沉淀铁离子和铝离子,但不能沉淀镁离子,所以根据沉淀的pH可知,应控制溶液pH的合理范围是7~8,答案选C。
(3)检验铁离子的试剂是KSCN溶液,即取少量溶液Ⅱ于试管中,加入KSCN溶液,若无明显现象,说明溶液Ⅱ不含Fe3+;若溶液变红色,说明溶液Ⅱ含有Fe3+。
(4)B中沉淀是氢氧化铝和氢氧化铁,由于氢氧化铝是两性氢氧化物,所以得到氢氧化铁的方法是加入氢氧化钠溶液,过滤即可,反应的离子方程式是OH-+Al(OH)3 = AlO2-+2H2O;由于在氢氧化铁表面有吸附的离子,所以在过滤之后还需要洗涤,最后加热或灼烧。
本题难度:一般
3、选择题 从实验安全角度考虑,下列操作错误的是?(?)
A.不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛
B.不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗
C.若苯酚溶液沾到皮肤上,应立即用大量水冲洗
D.配制浓硫酸和乙醇混合液时,先将浓硫注入烧杯中,然后,边加无水酒精边用玻璃棒搅拌至冷却
参考答案:D
本题解析:D错,配制浓硫酸和乙醇混合液时,先将无水乙醇注入烧杯中,然后,边加浓硫酸边用玻璃棒搅拌至冷却;
本题难度:一般
4、选择题 从化学试剂商店购买的某些试剂瓶上常贴有危险化学品的标志。盛装氢氧化钠的试剂瓶上所贴的危险化学品标志是(?)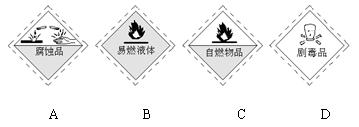
参考答案:A
本题解析:略
本题难度:简单
5、选择题 下列实验操作与实验目的或结论一致的是
| 选项 | 实验操作 | 实验目的或结论 |
| A | 向某溶质中先滴加稀硝酸酸化,再滴加BaCl2溶液,有白色沉淀生成 | 该溶液中一定含有Ag+ |
| B | 将混合气通过饱和的Na2CO3溶液 | 除去CO2中混有的HCl |
| C | 配制SnCl2溶液时,先将SnCl2溶于适量的稀盐酸中,再用蒸馏水稀释,保存时在试剂瓶中加入少量的锡粒 | 抑制Sn2+水解,并防止Sn2+被氧化为Sn4+ |
| D | 将苯滴入溴水中,振荡,静置,溴水层褪色 | 溴或苯发生加成反应 |
参考答案:C
本题解析:A、向某溶质中先滴加稀硝酸酸化,再滴加BaCl2溶液,有白色沉淀生成,该白色沉淀可能是氯化银,也可能是硫酸钡,所以不能确定溶液中是否一定含有Ag+,A不正确;B、除去CO2中的HCl气体,应该将混合气通过饱和的NaHCO3溶液,而不能通过饱和的Na2CO3溶液,因为Na2CO3溶液也吸收CO2气体,B不正确;C、由于Sn2+在溶液中易水解,且易被氧化生成Sn4+,所以配制SnCl2溶液时,先将SnCl2溶于适量的稀盐酸中,再用蒸馏水稀释,保存时在试剂瓶中加入少量的锡粒,以防止Sn2+水解,并为防止Sn2+被氧化为Sn4+,C正确;D、单质溴易溶在苯中,因此将苯滴入溴水中,振荡发生的时萃取,而不是加成反应,D不正确,答案选C。
本题难度:一般