时间:2020-07-08 00:38:03
1、选择题 用石墨电极在一定温度下电解K2SO4饱和溶液m?g.当阴极产生a?mol气体时,从溶液中析出n?g无水晶体.则剩余溶液的溶质质量分数是( )
A.
| n 18a+n |
| n m-n |
| n 9a+n |
| n 36a+n |
2、选择题 可以将反应Zn+Br2 = ZnBr2设计成蓄电池,下列4个电极反应 ① Br2 + 2e-= 2Br- ② 2Br--2e-= Br2 ③ Zn - 2e-= Zn2+ ④ Zn2+ +2e-= Zn 其中表示充电时的阳极反应和放电时的负极反应的分别是
[? ]
A.②和③
B.②和①
C.③和①
D.④和①
3、选择题 用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得的溶液中加入 0.1molCu(OH)2后恰好恢复到电解前的浓度和PH。则电解过程中转移的电子数为(? )
A.0.1mol
B.0.2mol
C.0.3mol
D.0.4mol
4、填空题 电解原理常应用于工业生产
(1)火法炼铜得到的粗铜中含多种杂质(如锌、金、银等),其性能远不能达到电气工业的要求,工业上常使用电解精炼法将粗铜提纯。在电解精炼时,若用硫酸铜溶液作电解液,粗铜接电源?极,电极反应为?;通电一段时间后,溶液中铜离子浓度将?(增大,不变,减少)。
(2)工业上用电解饱和食盐水的方法可制得烧碱、氯气、氢气。电解时,总离子反应
式为?;电解时所需的精制食盐水,通常在粗盐水
加入某些试剂(现提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液来、BaCl2
溶液、Ba(NO3)2溶液、盐酸)除去其中的Ca2+、Mg2+、Fe3+、SO42-杂质离子,选出试剂,
按滴加的先后顺序为?(填所加试剂的化学式)。
(3)为了避免产物相混合发生副反应,工业上采用离子交换膜法电解食盐水。下图为阳离
子交换膜法电解饱和食盐水原理示意图。
5、选择题 烧碱的制备,在上世纪七十年代常用水银法,此法通过钠汞齐(Na・nHg)生产得到的烧碱质量好,浓度高,目前已被离子交换膜法所取代。两种生产方法示意图如下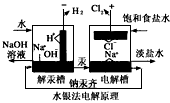

下列说法正确的是
[? ]
A.水银法被淘汰,是因为生产过程中,汞不能循环利用
B.水银法生产,在电解槽中,阴极的电极反应式为:Na++e-+nHg=Na・nHg
C.离子膜法电解,阳极发生的电极反应为:2H++2e-=H2↑
D.水银法中烧碱在电解槽中生成,离子膜法烧碱在阴极生成