时间:2020-07-08 00:22:37
1、选择题 理论上不能用于设计成原电池的反应是
A.HCl+NaOH===NaCl+H2OΔH<0
B.2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l)ΔH<0
C.4Fe(OH)2(s)+2H2O(l)+O2(g)===4 Fe(OH)3(s)ΔH<0
D.2H2(g)+O2(g)===2H2O(l) ΔH<0
2、选择题 木炭与浓硫酸反应可表示为:C +2H2SO4(浓)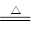 CO2↑+2SO2↑+2H2O。
CO2↑+2SO2↑+2H2O。
(1)该反应的反应物和生成物中,属于氧化物的是 。
(2)木炭作 (填“氧化剂”或“还原剂”),硫酸 (填“被氧化”或“被还原”)。
(3)若消耗了2mol H2SO4,则生成 mol SO2。
3、选择题 下列反应属于氧化还原反应的是 ( )
A.CaCO3+2HCl===CaCl2+CO2↑+H2O
B.CO2+H2O===H2CO3
C.2H2O2催化剂 2H2O+O2↑
D.CaCO3 CaO+CO2↑
CaO+CO2↑
4、选择题 下列反应中属于氧化还原反应,但水既不做氧化剂,又不做还原剂的是
A.ICl+H2O=HCl+HIO
B.2K+2H2O=2KOH+H2↑
C.2F2+2H2O=4HF+O2
D.2Na2O2+2H2O=4NaOH+O2
5、选择题 下列化学名词书写正确的是
A.畜电池
B.脂化反应
C.油脂
D.铵基酸