时间:2020-07-08 00:05:27
1、选择题 下列溶液中的Cl-浓度与50 mL 1 mol·L-1 MgCl2溶液中的Cl-浓度相等的是
A.150 mL 1 mol·L-1 NaCl溶液
B.75 mL 2 mol·L-1 CaCl2溶液
C.150 mL 2 mol·L-1 KCl溶液
D.75 mL 1 mol·L-1 AlCl3溶液
2、填空题 3.6克的H2O的物质的量是______,分子个数是_______;质量相等的?CO?和?CO2?中,原子个数之比为______.
3、选择题 设NA为阿伏加德罗常数,下列说法中正确的是
A.标准状况下,密度为d g/L的某气体纯净物一个分子的质量为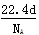 g
g
B.常温常压下,17g甲基(—14CH3)所含的中子数为9NA
C.25℃时,1 L pH=13的NaOH溶液中含有NA个氢氧根离子
D.4.6 g Na在空气中完全反应生成Na2O、Na2O2,转移0.2NA个电子
4、选择题 将153.5g由氯化钠和氯化镁混合而成的盐溶解于水配成1L溶液,测得溶液中Cl-的浓度为3mol/L,则溶液中Na+的物质的量浓度为( )
A.2mol/L
B.1mol/L
C.0.5mol/L
D.0.1mol/L
5、选择题 下列说法正确的是(设阿伏加德罗常数的数值为6.02×1023)
A.在标准状况下,22.4L苯所含分子数目为6.02×1023
B.1mol/LK2SO4溶液所含K+数目为6.02×1023
C.2g氢气所含的原子数为NA
D.在常温常压下,16gO2和O3的混合气体所含原子数目为6.02×1023