时间:2020-07-07 23:58:51
1、选择题 在0.1mol/L的氨水中存在 NH3·H2O  ?NH4++OH-的电离平衡,下列措施都能使该平衡向右移动的一组是 (? )
?NH4++OH-的电离平衡,下列措施都能使该平衡向右移动的一组是 (? )
①加入少量HCl? ②加入固体NaOH? ③加水? ④通入氨气
⑤加热升高温度? ⑥加入NH4NO3
A.①③④⑤
B.①③④⑤⑥
C.②③④⑤
D.①③④⑥
参考答案:A
本题解析:向氨水中加入盐酸,H+与OH-反应,平衡向右移动;加氢氧化钠固体,c(OH-)增大,平衡向左移动;加水稀释,促进电离,平衡向右移动;通入氨气,c(NH3·H2O)增大,平衡向右移动;电离过程是吸热过程,升高温度,平衡向右移动;加入硝酸铵,c(NH4+)增大,平衡向左移动。
点评:勒沙特列原理同样适用于弱电解质电离平衡。
本题难度:一般
2、填空题 将6g CH3COOH溶于水制成1L溶液,此溶液的物质的量浓度为_______,经测定溶液中含CH3COO -为1.4× 10-3 mol·L-1,此温度下醋酸的电离常数:Ka=__________,升高温度,Ka将___________(填“变大”“不变”或“变小”)。
参考答案:0.1 mol·1-1 ;1.96×10-5mol·L-1 ;变大
本题解析:
本题难度:一般
3、选择题 已知HCN、CN—在溶液中存在下列平衡及其对应的平衡常数:
①HCN H++CN— △H1>0 K1
H++CN— △H1>0 K1
②CN—+H2O HCN+OH- △H 2>0 K2
HCN+OH- △H 2>0 K2
常温下(K1=6.2×10-10),将等体积、等物质的量浓度的HCN和NaCN溶液混合,下列叙述正确的是
A.混合溶液的pH<7
B.对混合溶液进行微热,K1增大、K2减小
C.K2≈ 1.6×10-5
D.c(Na+) =" c(HCN)" + c(CN?)
参考答案:C
本题解析:A.由于不能确定HCN的电离程度与CN—的水解程度的相对大小,因此不能确定溶液的酸碱性,则混合溶液的pH不一定小于7,A错误;B.水解和电离都是吸热的,所以对混合溶液进行微热,K1、K2均增大,B错误;C.K2=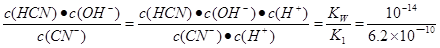 ≈1.6×10-5,C错误;D.根据物料守恒可知2c(Na+)=c(HCN) + c(CN?),D错误,答案选C。
≈1.6×10-5,C错误;D.根据物料守恒可知2c(Na+)=c(HCN) + c(CN?),D错误,答案选C。
考点:考查溶液酸碱性、水解常数、物料守恒以及外界条件对电离平衡和水解平衡的影响
本题难度:困难
4、选择题 关于pH相同的醋酸和盐酸溶液,下列叙述不正确的是
A.取等体积的两种酸溶液分别进行稀释至原溶液的m倍和n倍,结果两溶液的pH仍然相同,则m>n
B.取等体积的两种酸溶液分别与完全一样的足量锌粒反应,开始时反应速率盐酸大于醋酸
C.取等体积的两种酸溶液分别中和NaOH溶液,醋酸消耗NaOH的物质的量比盐酸多
D.两种酸溶液中c(CH3COO-)=c(Cl-)
参考答案:B
本题解析:考查弱电解质的电离平衡
A:两溶液稀释相同倍数时,由于促进了弱酸的电离平衡,可电离出部分氢离子,醋酸的pH将小于盐酸,故为保证pH相同,醋酸稀释倍数应相对较大,正确
B:开始反应是两溶液的氢离子浓度相同,反应速率也应该相同,不正确
C:由于在中和过程中,醋酸可不断电离出氢离子,故醋酸消耗的碱相对多,正确
D:两溶液中分别存在电荷守恒:c(CH3COO-)+c(OH-)=c(H+)、c(Cl-)+c(OH-)=c(H+),由于两溶液的pH相同,可得出c(CH3COO-)=c(Cl-),正确
答案为B
本题难度:简单
5、选择题 下列溶液中各微粒的浓度关系不正确的是( )
A.0.1?mol/LHCOOH溶液中:c(HCOO-)+c(OH-)═c(H+)
B.1?L?0.1?mol/LCuSO4?(NH4)2SO4?6H2O的溶液中:c(SO42-)>c(NH4+)>c(Cu2+)>c(H+)>c(OH-)
C.0.1?mol/L?NaHCO3溶液中:c(Na+)+c(H+)+c(H2CO3)═c(HCO3-)+c(CO32-)+c(OH-)
D.等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-)
参考答案:A、0.1 mol/LHCOOH溶液中存在电荷守恒:c(HCOO-)+c(OH-)═c(H+),故A正确;
B、铵根离子水解呈酸性,1 L 0.1 mol/LCuSO4?(NH4)2SO4?6H2O的溶液中:c(SO42-)>c(NH4+)>c(Cu2+)>c(H+)>c(OH-),故B正确;
C、0.1 mol/L NaHCO3溶液中存在电荷守恒:c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-),故C错误;
D、等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液中,X-的水解程度和HX的电离程度不同,溶液的酸碱性不同,电离大于水解,溶液呈酸性,电离小于水解,溶液呈碱性,故D错误;
故选CD.
本题解析:
本题难度:一般