ʱ��:2020-07-07 23:53:14
1��ѡ���� ���и��������У����۵��ɵ͵���������ȷ���ǣ�?��
A��O2��I2��Hg
B��CO2��KCl��SiO2
C��HF��HCl��HI
D��SiO2��NaCl��SO2
2��ѡ���� 2011��ŵ������ѧ��������ɫ�п�ѧ�Ҵ��ᰣ����л���������Ա��������������塣������Ͼ���Ӳ�ȸߣ��������ˣ�ʹ�����������ص㡣��������������ǣ�?��
A����Ȼ���еĹ���ɷ�Ϊ���塢����ͷǾ�̬����
B��������һ�ֽ��ھ���ͷǾ�̬����֮��Ĺ���
C��������ϵ�Ӧ�þ��нϴ�ķ�չ�ռ�
D����ѧʽΪAl63Cu24Fe13�����岻����ϡ���ᷢ����Ӧ
3��ѡ���� �����������й����ʵ������У��������ڽ����������(? )
A���ɷ��Ӽ���������϶��ɣ��۵��
B����������ں����磬�۵���1000������
C���ɹ��ۼ���ϳ���״�ṹ���۵��
D�����岻���磬������ˮ�����ں��ܵ���
4��ѡ���� ��ͼ�Ǵ�NaCl��CsCl����ṹͼ�зָ�����IJ��ֽṹͼ���������ڴ�NaCl�����зָ�����Ľṹͼ�ǣ� ? ��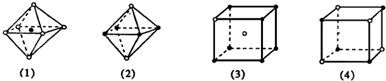
A��ͼ��1����ͼ��3��
B��ͼ��2����ͼ��3��
C��ͼ��1����ͼ��4��
D��ֻ��ͼ��4��
5������� ?����ѧ�D�Dѡ�����ʽṹ�����ʡ���15�֣�
��A��B��C��D��E����Ԫ�ء��������Ϣ���£�
��ش��������⡣
(1) д��EԪ��ԭ�ӻ�̬ʱ�ĵ����Ų�ʽ__________________��
(2) CԪ�صĵ�һ�����ܱ���Ԫ���ĵ�һ������ ______ ______ (���С��)��
(3) CA3������Cԭ�ӵ��ӻ����������____________��
(4) A��C��E����Ԫ�ؿ��γ�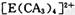 �����ӣ����д��ڵĻ�ѧ�������� ______ (����ţ���
�����ӣ����д��ڵĻ�ѧ�������� ______ (����ţ���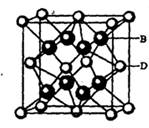
����λ�� �ڽ������ۼ��Թ��ۼ��ܷǼ��Թ��ۼ������Ӽ� �����
��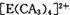 ���жԳƵĿռ乹�ͣ��ҵ�
���жԳƵĿռ乹�ͣ��ҵ�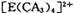 �е�����CA3������Cl-ȡ��ʱ���ܵõ����ֲ�ͬ�ṹ�IJ����
�е�����CA3������Cl-ȡ��ʱ���ܵõ����ֲ�ͬ�ṹ�IJ���� �Ŀռ乹��Ϊ ____________ (�����)��
�Ŀռ乹��Ϊ ____________ (�����)��
a.ƽ��������b.��������c.������ ?d. V��
(5) B��D���γ����ӻ�����,�侧���ṹ����ͼ��ʾ������D���ӵ���λ��Ϊ_____,���þ�����ܶ�Ϊag ? cm��3,��þ����������______cm-3(д������ʽ����)��