ʱ��:2020-07-07 23:36:52
1��ѡ���� ����NaBr��KI����Һ��ͨ�������Cl2��Ȼ����Һ���ɣ������չ��壬���õ��������ǣ�?��
A��KCl
B��NaCl��KCl
C��NaCl��KBr
D��NaCl��KCl��I2
�ο��𰸣�B
���������ͨ�����Cl2��������Ӧ2NaBr+Cl2====2NaCl+Br2��2KI+Cl2====2KCl+I2����������ʱBr2�ӷ���I2������
�����Ѷȣ���
2��ʵ���� ����������Ũ�����ϼ��ȵõ���������ͼ����ȡ��̽��Cl2��ѧ���ʵ�װ��ͼ��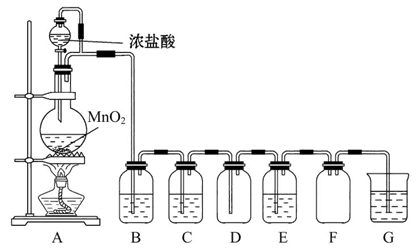
��1��Բ����ƿ�з�����Ӧ�Ļ�ѧ����ʽΪ________��
��2����Ҫ�õ����﴿�������壬B��C��Ӧ�ֱ�ʢ�ŵ��Լ�Ϊ________��________��
��3��E����װ��FeCl2��Һ����Ӧ�����ӷ���ʽΪ________��E����װ�е��۵⻯����Һ���ܹ۲쵽��ʵ��������______________________________________��
��4��ʵ���з��֣�Ũ������MnO2��ϼ�������������ϡ������MnO2��ϼ��Ȳ����������������������ij��ѧ��ȤС��ԡ�Ӱ���������ɵ�ԭ���������ۣ������������ʵ�鷽����
a��ϡ�������MnO2�У�Ȼ��ͨ��HCl�������
b��ϡ�������MnO2�У�Ȼ�����NaCl�������
c��ϡ�������MnO2�У�Ȼ�����Ũ�������
d��MnO2��NaCl��Ũ��Һ��ϼ���
e��Ũ������NaCl���塢MnO2���干��
��ʵ��b��Ŀ����__________________________________________��
ʵ��c��Ŀ����_________________________________________________��
��ʵ������a��c��e�л���ɫ�������ɣ�b��dû�л���ɫ�������ɡ��ɴ˵ó�Ӱ���������ɵ�ԭ����____________________________________________��
�ο��𰸣���1��MnO2+4HCl��Ũ��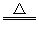 MnCl2+Cl2��+2H2O
MnCl2+Cl2��+2H2O
��2������ʳ��ˮ?Ũ����
��3��2Fe2++Cl2=2Fe3++2Cl-?��Һ����
��4����̽��c��Cl-���Է�Ӧ��Ӱ��?̽��c��H+���Է�Ӧ��Ӱ��?��c��H+���Ĵ�С
�����������1��MnO2��Ũ���ᷴӦ�Ļ�ѧ����ʽΪ��MnO2+4HCl��Ũ�� MnCl2+
MnCl2+
Cl2��+2H2O��
��2���ø÷����Ƶõ������к���HCl��ˮ�������ֱ��ñ���ʳ��ˮ��Ũ�����ȥ��
��3��������FeCl2��Һ��Ӧ�����ӷ���ʽ�ǣ�2Fe2++Cl2=2Fe3++2Cl-��������KI����Ϊ���ʵ⣬���ʵ�ʹ���۱���ɫ��
��4���Ա�a��b��c��d��e���ʵ�鷽�����Կ��������ʵ���ж���MnO2��Cl-��ֻ��a��c��e���нϴ�Ũ�ȵ�H+��������ʵ�������Cl2��b��d���нϴ�Ũ�ȵ�Cl-������H+��û�в���Cl2��˵��Ӱ���������ɵ�ԭ����H+Ũ�ȵĴ�С��ʵ��b��Ŀ����̽��c��Cl-���Է�Ӧ��Ӱ�죬ʵ��c��Ŀ����̽��c��H+���Է�Ӧ��Ӱ�졣
�����Ѷȣ�һ��
3��ѡ���� ����˵���У���ȷ���ǣ�������
A��������Fe��Cl2��ַ�Ӧ������FeCl2
B������CO2ͨ��BaCl2��Һ�����ɰ�ɫ����
C�������ó���ʯ��ˮ�����մ��С�մ�
D��Na2O2�ͻ���̿����ʹƷ����Һ��ɫ������ɫԭ����ͬ
�ο��𰸣�A������������ȼ�գ����������Ƿ������ֻ�����Ȼ�������A����
B����������Դ���̼�ᣬ���Զ�����̼���Ȼ�����Һ����Ӧ����B����
C��Na2CO3+Ca��OH��2�TCaCO3��+2NaOH��2NaHCO3+Ca��OH��2�TCaCO3��+Na2CO3+2H2O�������ְ�ɫ�����������𣬹�C����
D���������ƾ���ǿ�����ԣ�����̿���������ԣ���������ʹƷ����ɫ�����ù������Ƶ�ǿ�����ԣ�����̿ʹƷ����Һ��ɫ�����û���̿�������ԣ�������ɫԭ����ͬ����D��ȷ��
��ѡD��
���������
�����Ѷȣ�һ��
4������� ijѧУ��ѧѧϰС��Ϊ̽���������������ʣ�����ͼ��ʾװ�ý���ʵ�顣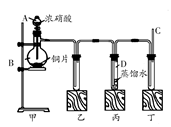
��ش��������⣺
(1)װ�ü���ʢ��Ũ���������A��������?����װ���з�����Ӧ�Ļ�ѧ����ʽΪ?��
(2)ʵ������У�װ���ҡ����г��ֵ�����ֱ���?��װ�ñ��е��Թ��ڷ�����Ӧ�����ӷ���ʽΪ?��
(3)Ϊ��̽��NO�Ļ�ԭ�ԣ�������װ�ö��ĵ�����C��ͨ��һ�����壬ͨ������������������?��
(4)ȡ��װ�ñ��е��Թ�D�������еμ�FeSO4��Һ����Һ��Ϊ?ɫ��Ϊ��֤����Ԫ���ڸ÷�Ӧ�еIJ������������Һ�еμ�KSCN��Һ����Һ��Ϊ?ɫ��
�ο��𰸣�(1)��Һ©��(��©�����÷�)? Cu��4HNO3(Ũ)=Cu(NO3)2��2NO2����2H2O
(2)���ֺ���ɫ���� ������ɫ���塢����ˮ��������?3NO2��H2O=2H����2NO��NO
(3)����
(4)�� ��
���������(1)��Ũ������ͭ�ķ�Ӧ�У���Ҫ��ʱ����Ũ������������ʲ��÷�Һ©����������һ���©����Ũ������ͭ��Ӧ���ɶ���������
(2)��������Ϊ����ɫ���壬�ܹ���ˮ��Ӧ������ɫ��һ��������
(3)һ��������������Ӧ���ֻ�ԭ�ԣ�������Ϊ����������
(4)�Թ�D�е���ҺΪϡ���ᣬϡ������������ԣ��ܹ���������������Ϊ�����ӣ���������SCN�����ɺ�ɫ�����ʡ�
�����Ѷȣ�һ��
5�������� ��9�֣���a g������b g�����ϳ��Ȼ������壬Ȼ��Ӧ�������������������������Һ������գ��Ը�����������������ȵIJ�ͬ������ۣ�
��1�����պ�ʣ���������������2�����պ�����ʳ�ε�������
�ο��𰸣�(1)��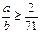 ʱ����H2(
ʱ����H2(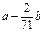 )g��ʳ�ε�������
)g��ʳ�ε�������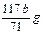 ?
?
(2)��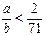 ʱ��������ʣ�࣬ʳ�ε�������
ʱ��������ʣ�࣬ʳ�ε�������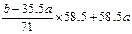
���������H2?��? Cl2?��? 2HCl?��? 2NaCl
2g? 71g? 73g? 117g
ag? bg? m(HCl)? m(NaCl)
(1)��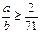 ʱ����H2(
ʱ����H2(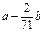 )g��ʳ�ε�������
)g��ʳ�ε�������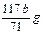
(2)��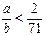 ʱ����Cl2��b-35.5a��g������ʳ�ε�����Ϊ58.5g���������Cl2�ֱ�������NaOH��Һ���գ�������NaCl��NaClO������Cl2?�� NaCl��֪������ʳ��
ʱ����Cl2��b-35.5a��g������ʳ�ε�����Ϊ58.5g���������Cl2�ֱ�������NaOH��Һ���գ�������NaCl��NaClO������Cl2?�� NaCl��֪������ʳ��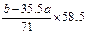 g����������������ʣ�࣬ʳ�ε�������
g����������������ʣ�࣬ʳ�ε�������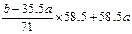
�����Ѷȣ���