时间:2020-07-07 23:25:36
1、选择题 下列图示与对应的叙述相符的是



图Ⅰ 图Ⅱ 图Ⅲ 图Ⅳ
A.图Ⅰ表示t℃时冰醋酸在稀释过程中溶液导电性的变化
B.图Ⅱ表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化
C.图Ⅲ表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强比甲的大
3C(g)+D(s)的影响,乙的压强比甲的大
D.据图Ⅳ,若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH在4左右
2、选择题 现有常温下的四种溶液(如下表),下列有关叙述中正确的是( )
| ① | ② | ③ | ④ 溶液 氨水 氢氧化钠溶液 醋酸 硫酸 pH 11 11 3 3 |
3、选择题 能够说明氨水是弱碱的事实是 ( )
A.氨水具有挥发性
B.1 mol・L-1氨水溶液pH≈ll
C.氨水溶液能导电
D.氨水与HCl溶液反应生成NH4Cl
4、填空题 现有浓度均为0.1mol?L-1的下列溶液:①硫酸.②醋酸.③氢氧化钠.④氯化铵.⑤醋酸铵.⑥硫酸氢铵.⑦氨水,请回答下列问题:
(1)①.②.③.④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)______.
(2)④.⑤.⑥.⑦四种溶液中NH4+浓度由大到小的顺序是(填序号)______.
(3)将③和④按体积比1:2混合后,混合液中各离子浓度由大到小的顺序是______.
(4)已知t℃时,Kw=1×10-13,则t℃(填“>”“<”或“=”)______25℃.
5、选择题 下列说法正确的是
[? ]
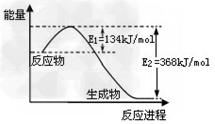
A.?已知1?mol?NO2和1?mol?CO反应生成CO2和NO过程中能量变化如图,则NO2和CO反应的热化学方程式为:NO2(g)+CO(g)=CO2(g)+NO(g);△H=?+234kJ/mol ?
B.?一定温度下,利用pH计测定不同浓度醋酸溶液的pH 值,得到数据(如上表)
当醋酸浓度为0.1mol/L时,通过计算求得该温度下醋酸的电离度为1%
C.?已知CaCO3的Ksp=2.8×10-9,现将等体积的Na2CO3溶液与CaBr2溶液混合,若CaBr2溶液的浓度为?5.6×10-5?mol/L,则生成沉淀所需Na2CO3溶液的最小浓度为?5×10-5mol/L
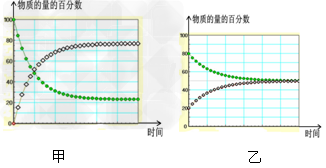
D.?在不同条件下进行的异构化反应?X Y?的进程图解。图中的“
Y?的进程图解。图中的“ ”是X,“
”是X,“ ”是Y 则可以计算得到乙的平衡常数K=1,且比甲的平衡常数要小
”是Y 则可以计算得到乙的平衡常数K=1,且比甲的平衡常数要小