时间:2020-07-07 23:14:04
1、选择题 对于原子序数为?116?号的元素X,下列叙述正确的是( )
A.X是非金属元素
B.X的最高价氧化物的化学式为:XO3
C.X的钠盐的化学式为:Na2X
D.X的最高价氧化物的水化物为强酸
参考答案:B
本题解析:
本题难度:简单
2、选择题 元素A的原子最外层有6个电子,元素B的原子最外层有3个电子,则A与B形成的化合物的化学式可能是
[? ]
A.A2B3
B.B2A3
C.B2A
D.A2B
参考答案:B
本题解析:
本题难度:简单
3、简答题 Q、W、X、Y、Z是5种短周期元素,原子序数逐渐增大,Q是周期表中原子半径最小的元素,Q与W组成的化合物是一种温室气体,W与Y、X与Y组成的化合物是机动车排出的大气污染物,Y和Z能形成原子个数比为1:1和1:2的两种离子化合物.
(1)W在元素周期表中的位置是______,Z2Y的电子式是______.
(2)①已知“凡气体分子总数增多的反应一定是熵增大的反应”.根据所学知识判断如下反应2WY(g)=2W(s)+Y2(g)△H>0,在常温下______自发进行(填“能”或“不能”).
②400℃时,在0.5L的反应容器中用X2、Q2反应合成XQ3反应,达到平衡时,测得X2、Q2、XQ3的物质的量分别为2mol、1mol、2mol,则此反应在400℃时的化学平衡常数为______
(3)2.24L(标准状况)XQ3被200mL?1mol/L?QXY3溶液吸收后,所得溶液中离子浓度从大到小的顺序是______.
(4)WQ4Y与Y2的反应可将化学能转化为电能,其工作原理如图所示,a极的电极反应式是______
(5)X和Z组成的一种离子化合物,能与水反应生成两种碱,该反应的化学方程式是______.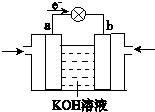
参考答案:Q是周期表中原子半径最小的元素,应为H,Q与W组成的化合物是一种温室气体,该气体为CH4,则W为C,W与Y、X与Y组成的化合物是机动车排出的大气污染物,为CO和NOx,则Y为O,X为N,Y和Z能形成原子个数比为1:1和1:2的两种离子化合物,这两种离子化合物分别为Na2O、Na2O2,作为Z为Na,则
(1)W为C,原子序数为6,原子核外有2个电子层,最外层电子数为6,应位于周期表第二周期IVA族,
Z2Y为Na2O,为离子化合物,电子式为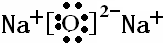
,
故答案为:第二周期IVA族;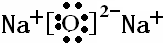
;?
(2)①由自由能判据△G=△H-T?△S,可知当△H<T?△S时反应才能自发进行,即必须在较高的温度下才可以进行,化学反应能否自发进行取决于焓变和熵变的综合判据,不能只由焓变或熵变来决定,故答案为:不能;
?②达平衡时,各物质的浓度分别为:c(N2)=4mol/L,c(H2)=2mol/L,c(NH3)=4mol/L,
则k=c2(NH3)c(N2)×c3(H2?)=424×23=0.5,故答案为:0.5;
(3)n(NH3)=2.24L22.4L/mol=0.1mol,n(HNO3)=0.2L×1mol/L=0.2mol,HNO3过量,生成NH4NO3,二者物质的量相等,但由于NH4+水解,则c(H+)>c(NH4+),所以溶液中存在c(NO3-)>c(H+)>c(NH4+)>c(OH-),
故答案为:c(NO3-)>c(H+)>c(NH4+)>c(OH-);?
(4)CH3OH碱性燃料电池中,CH3OH为电池的负极反应,被氧化,电极反应式为CH3OH+8OH--6e-=CO32-+6H2O,
故答案为:CH3OH+8OH--6e-=CO32-+6H2O;
(5)X和Z组成的一种离子化合物为Na3N,能与水反应生成两种碱,生成物为NaOH和NH3?H2O,反应的化学方程式为Na3N+4H2O=3NaOH+NH3?H2O,
故答案为:Na3N+4H2O=3NaOH+NH3?H2O.
本题解析:
本题难度:一般
4、选择题 下列说法中,不正确的是( )
A.原子最外层电子数比次外层电子数多的元素一定位于第二周期
B.从氟到碘,单质与氢气发生化合反应越来越难
C.14C和14N两种核素的质量数相同,中子数也相同
D.离子化合物中可能含有共价键,但共价化合物中一定不含离子健
参考答案:A、因第一层最多排2个电子,第二层最多排8个电子,第三层最多排布18个电子,且在每层最多容纳的电子数为2n2个时,同时符合最外层电子数不超过8个,倒数第二层不超过18个,显然原子最外层电子数比次外层电子数多的元素一定位于第二周期,故A正确;
B、从氟到碘非金属性逐渐减弱,则与氢气发生化合反应越来越难,故B正确;
C、14C的中子数为14-6=8,14N的中子数14-7=7,中子数不同,故C错误;
D、含有离子键的化合物一定是离子化合物,但离子化合物中可以含有共价键,如NaOH等,故D正确;
故选C.
本题解析:
本题难度:简单
5、选择题 X,Y,Z,R是1~18号元素中的4种元素,它们的原子结构有以下特点:
①X元素原子的M层比L层少3个电子,
②Y元素的-2价阴离子的核外电子排布与氖原子相同,
③Z元素原子的L层比M层多5个电子,
④R元素原子的L 层比K层多3个电子,
其中金属性最强的是
[? ]
A.X
B.Y
C.Z
D.R
参考答案:C
本题解析:
本题难度:一般