时间:2020-07-07 23:11:58
1、选择题 设阿伏加德罗常数的数值为,下列叙述正确的是
A.标准状况下,22.4L四氯化碳含有的分子数为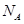
B.1 mol硫酸钾中阴离子所带的电荷数为2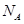
C.0.5 mol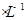 NaOH溶液中 Na+数为0.5
NaOH溶液中 Na+数为0.5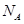
D.常温常压下,16g氧气所含电子数为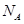
2、选择题 瓦斯中甲烷与氧气的质量比为1︰4时极易发生爆炸,则此时甲烷与氧气的体积比是(?)
A.1︰4
B.1︰2
C.1︰1
D.2︰1
3、实验题 (各2.5分,共5分).取一定量的Na2CO3和Na2SO4混合物溶液与过量盐酸反应,生成2.016 L CO2(标况下),然后加入足量的Ba(OH)2溶液,得到沉淀的质量为2.33 g。试计算混合物中Na2CO3和Na2SO4的物质的量分别为多少。
4、选择题 2molCl2和2molCO2相比较正确的是?
A.分子数相等
B.原子数相等
C.体积相等
D.质量相等
5、选择题 配制物质的量浓度的溶液,造成浓度偏高的操作是( )
A.定容时,滴加蒸馏水超过刻度线
B.定容时,眼睛俯视刻度线
C.洗涤烧杯和玻璃棒的溶液未转入容量瓶中
D.定容时,眼睛仰视刻度线