时间:2020-07-07 23:11:14
1、选择题 下列热化学方程式书写正确的是(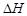 的绝对值均正确)
的绝对值均正确)
A.C2H5OH(l)+3O2(g)===2CO2(g)+3H2O(g)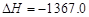 kJ/mol(燃烧热)
kJ/mol(燃烧热)
B.NaOH(aq)+HCl (aq)===NaCl (aq) +H2O(l)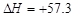 kJ/mol(中和热)
kJ/mol(中和热)
C.S(s)+O2(g)===SO2(g)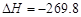 kJ/mol(反应热)
kJ/mol(反应热)
D.Fe+S===FeS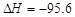 kJ/mol(反应热)
kJ/mol(反应热)
2、选择题 下列溶液一定呈酸性的是
A.pH=6的溶液
B.含有H?+的溶液
C.遇酚酞显无色的溶液
D.c(H+)>c(OH-)的溶液
3、填空题 (2分)用标准的NaOH滴定未知浓度的盐酸,选用酚酞为指示剂,造成测定结果偏高的原因可能是?。
A.滴定终点读数时,俯视滴定管的刻度,其它操作均正确;
B.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗;
C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液;
D.未用标准液润洗碱式滴定管;
4、实验题 (1)常温下,0.1 mol/L的醋酸和0.1 mol/L的盐酸各100 mL,分别与足量的锌粒反应,产生的气体体积前者?后者(填“<”、“>”或“=”).
(2)在25℃条件下将pH=5的氯化铵溶液稀释100倍 ,稀释后溶液的pH为(填选项字母,下同)?.
,稀释后溶液的pH为(填选项字母,下同)?.
A.5? B.7 ?C.3~5之间? D.5~7之间
(3)将体积和物质的量浓度都相同的醋酸和氢氧化钠溶液混合后,溶液呈?性(填“酸”,“中”或“碱”,下同),溶液中c(Na+)?c(CH3COO-)(填“ >” 或“=”或“<”,下同 )。
(4)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈?性,溶液中c(Na+)?c(CH3COO-)
(5)将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后溶液的pH=7,则醋酸溶液中c(H+)?氢氧化钠溶液中c(OH-),m与n的大小关系是m?n。
(6)用标准的NaOH滴定未知浓度的盐酸,选用酚酞为指示剂,造成测定结果偏高的原因可能是?。(多选、错选不得分)
A.配制标准溶液的氢氧化钠中混有Na2CO3杂质;
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确;
C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗;
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液;
E.未用标准液润洗碱式滴定管。
5、填空题 (14分)
(1)25 ℃时,将pH=11的NaOH溶液与pH=4的硫酸溶液混合,若所得混合溶液pH=9,则NaOH溶液与硫酸溶液的体积比为?
已知25 ℃时,0.1 L 0.1 mol・L-1的NaA溶液的pH=10,溶液中各离子的物质的量浓度由大到小的顺序为?。
(2))若100 ℃时,KW=10-12,则100 ℃时pH=11的Ba(OH)2溶液与pH=2的硫酸按体积比1:9混合充分反应后pH=?;若该温度下10体积的pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈中性,则混合之前,a与b之间应满足的关系为? ?。
?。
(3)某温度下的水溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L。x与y的关系如图所示。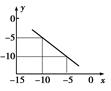
该温度下水的离子积为?。该温度下氯化钠溶液的pH为?
该温度下0.01 mol/L NaOH溶液的pH为?。