时间:2020-07-07 23:01:19
1、填空题 23.0.5mol H2SO4的质量是?g,含?个原子,含?mol氧原子.
参考答案:49;? 3.5NA;? 2
本题解析:硫酸的摩尔质量是98g/mol,所以0.5mol H2SO4的质量是0.5mol×98g/mol=49g。其中含有氧原子是0.5mol×4=2mol,总的原子的物质的量是0.5mol×(1×2+1+1×4)=3.5mol,所以原子数为3.5NA。
本题难度:一般
2、选择题 下列说法正确的是 ( )
①标准状况下,22.4 L己烯含有的分子数为6.02×1023
②标准状况下,a L的氧气和氮气的混合物含有的分子数约为a/22.4×6.02×1023
③7.1 g氯气与足量的氢氧化钠溶液反应转移的电子数约为0.2×6.02×1023
④60 g SiO2晶体中含有2×6.02×1023个Si-O键
⑤1 mol乙醇中含有的共价键数约为7×6.02×1023
⑥500 mL 1 mol・L-1的硫酸铝溶液中含有的硫酸根离子数约为1.5×6.02×1023
A.①④
B.②⑥
C.③⑤
D.②⑤
参考答案:B
本题解析:①错,己烯在标准状况下不是气体;②正确,根据关系式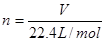 可得标准状况下,a L的氧气和氮气的混合物含有的分子数约为a/22.4×6.02×1023 ;③错,7.1 g氯气与足量的氢氧化钠溶液反应转移的电子数约为0.1×6.02×1023 ;④错60 g SiO2晶体中含有4×6.02×1023个Si-O键 ;⑤错,1 mol乙醇中含有的共价键数约为8×6.02×1023 ;
可得标准状况下,a L的氧气和氮气的混合物含有的分子数约为a/22.4×6.02×1023 ;③错,7.1 g氯气与足量的氢氧化钠溶液反应转移的电子数约为0.1×6.02×1023 ;④错60 g SiO2晶体中含有4×6.02×1023个Si-O键 ;⑤错,1 mol乙醇中含有的共价键数约为8×6.02×1023 ;
⑥正确,500 mL 1 mol・L-1的硫酸铝溶液中含有的硫酸根离子数约为1.5×6.02×1023
本题难度:一般
3、选择题 NA表示阿伏加德罗常数,下列说法正确的是
A.标准状况下,等体积的水和CO2,含有的氧原子数目为1∶2
B.含有NA个阴离子的Na2O2与足量水反应,转移电子数为2NA
C.向FeI2溶液中通入适量氯气,当有NA个Fe2+被氧化时,共转移电子数为3NA
D.一个NO分子质量为a g,一个NO2分子质量是b g,则NA个O2的质量为(b―a)NAg
参考答案:C
本题解析:略
本题难度:一般
4、选择题 相对分子质量为M的气态化合物VL(已换算成标准状况)溶于m g水中,得到溶液的溶质质量分数为ω%,物质的量浓度为c mol/L,密度为ρg・cm-3,则下列说法正确的是?
A.相对分子质量M可表示为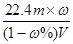
B.物质的量浓度C可表示为: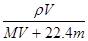
C.溶液的质量分数ω可表示为: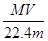
D.溶液密度p可表示为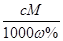
参考答案:D
本题解析:A错,标准状况下VL气态化合物的物质的量为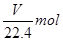 ;质量为
;质量为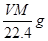 ,所以得
,所以得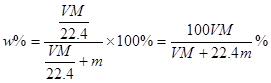
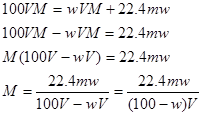
B错,气体的物质的量为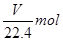 ,溶液的质量为
,溶液的质量为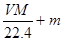 ,溶液的体积
,溶液的体积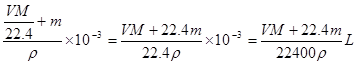 ,所以物质的量浓度为
,所以物质的量浓度为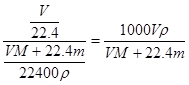
C错,溶液的质量分数: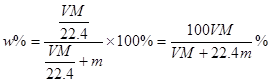
D正确,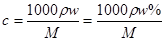 ;得
;得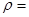
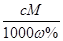
本题难度:简单
5、计算题 某化合物的化学式可表示为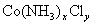 (x、y为正整数)。为了确定x和y的值,取两份质量均为0.2140g的该化合物进行如下两个实验。将一份试样溶于水,在硝酸存在的条件下用
(x、y为正整数)。为了确定x和y的值,取两份质量均为0.2140g的该化合物进行如下两个实验。将一份试样溶于水,在硝酸存在的条件下用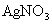 溶液滴定(生成
溶液滴定(生成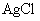 沉淀),共消耗24.0mL 0.100mol/L的
沉淀),共消耗24.0mL 0.100mol/L的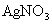 溶液。在另一份试样中加入过量
溶液。在另一份试样中加入过量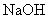 溶液并加热,用足量盐酸吸收逸出的
溶液并加热,用足量盐酸吸收逸出的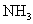 。吸收
。吸收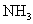 共消耗24.0mL 0.200mol/L
共消耗24.0mL 0.200mol/L 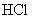 溶液。试通过计算确定该化合物的化学式。(本题可能用到的相对原子质量:H为1.00、N为14.0、Cl为35.5、Co为58.9)
溶液。试通过计算确定该化合物的化学式。(本题可能用到的相对原子质量:H为1.00、N为14.0、Cl为35.5、Co为58.9)
参考答案:解答:n表示物质的量,m表示质量
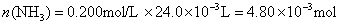
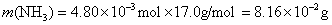
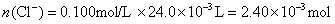
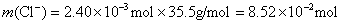
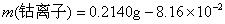
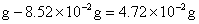
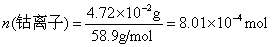
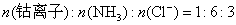
该化合物的化学式为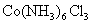 。
。
启示:同一习题,提倡一题多解,培养发散思维能力。如本题亦可有如下解法:
解法1:设0.2140g化合物的物质的量为n,根据关系式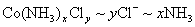 ,得方程:
,得方程:
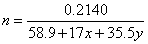 ①
①
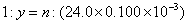 ②
②
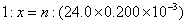 ③
③
联立①②③,解之得: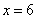 ,
,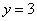 。
。
该化合物的化学式为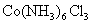 。
。
解法2:n表示物质的量,
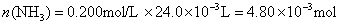
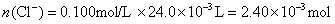
根据题意列方程组:
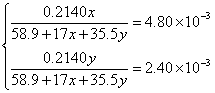 ?解方程组得:
?解方程组得: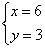
该化合物的化学式为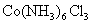 。
。
解法3:n表示物质的量。
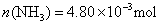
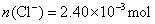
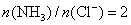 ?即:
?即: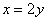
该化合物化学式可写成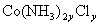 ,由题意得:
,由题意得:
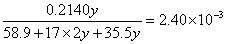 ?解之得:
?解之得: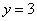
该化合物的化学式为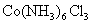 。
。
解法4:设0.2140g化合物的物质的量为c。
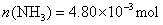
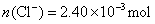
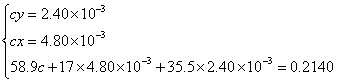
解联立方程得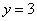 ,
,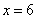 ,所以,其化学式为
,所以,其化学式为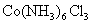 。
。
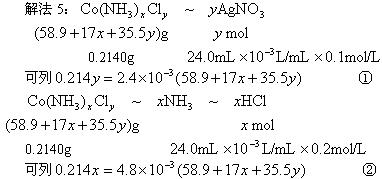
联立①、②解得: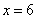 ,
,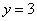 ,故化学式为
,故化学式为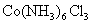 。
。
本题解析:此题有多种解法,训练学生的发散思维。
从消耗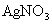 的物质的量可得化合物中
的物质的量可得化合物中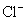 的物质的量;由吸收
的物质的量;由吸收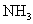 所消耗
所消耗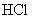 的物质的量可得
的物质的量可得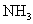 的物质的量,由试样质量减去
的物质的量,由试样质量减去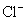 和
和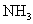 的质量可得钴离子的质量,除以钴的相对原子质量即得钴离子的物质的量。以钴离子的物质的量为1,即可确定x和y。
的质量可得钴离子的质量,除以钴的相对原子质量即得钴离子的物质的量。以钴离子的物质的量为1,即可确定x和y。
本题难度:简单